
| A、②③⑤ | B、①④⑥ |
| C、①②④⑥ | D、①②③④⑤⑥ |


科目:高中化学 来源: 题型:
| A、夏天冰镇啤酒倒入杯中,泛起大量泡沫 |
| B、氯水保存要在低温暗处 |
| C、工业上制氨要用高温,催化剂 |
| D、为提高SO2转化成SO3的量,常通入过量氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V1>V2>V3>V4 |
| B、V1>V3>V2>V4 |
| C、V2>V4>V3>V1 |
| D、V3>V1>V4>V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
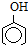 )>K2(H 2CO3),且知苯甲酸酸性比碳酸强,水杨酸(
)>K2(H 2CO3),且知苯甲酸酸性比碳酸强,水杨酸(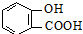 )与碳酸钠溶液反应生成CO2的同时,不能生成的物质是( )
)与碳酸钠溶液反应生成CO2的同时,不能生成的物质是( )A、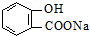 |
| B、NaHCO3 |
C、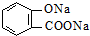 |
| D、H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.下列说法正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.下列说法正确的是( )| A、元素Q的非金属性比R的强 |
| B、离子半径的大小顺序:r(Tm+)>r(Wn-) |
| C、元素Q的氧化物均为酸性氧化物 |
| D、元素T与元素R的最高正价之和等于8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、油脂属于酯类,是高级脂肪酸的甘油酯 |
| B、油脂没有固定的熔、沸点 |
| C、油脂在不同条件下水解都能生成甘油 |
| D、油脂都不能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在1 L 0.2 mol?L-1的Na2CO3溶液中含有CO32-的数目为0.2NA |
| B、0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.3 NA |
| C、15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.2NA |
| D、1 mol Na2O2中含有的阴离子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、亚硝酸盐是还原剂 |
| B、维生素C是氧化剂 |
| C、维生素C将Fe3+还原为Fe2+ |
| D、亚硝酸盐被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com