
| A、标准状况下,11.2 L氦气中含有0.5 NA原子 |
| B、常温常压下,46g NO2和N2O4混合气体中含有原子总数为3NA |
| C、标准状况下,0.1 mol Cl2参加反应,转移的电子数目一定为0.2 NA |
| D、1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移电子总数NA个 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、原混合溶液中只存在Na+、Fe3+、SO42-,不可能存在K+、CO32- |
| B、由实验①无法推断原混合溶液中是否含有SO42- |
| C、由实验①、②可判断原混合溶液中是否含有Fe3+ |
| D、由实验③可判断原混合溶液中存在Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入澄清石灰水除去NaHCO3溶液中混有的少量Na2CO3 |
| B、常温下,pH=1的水溶液中NO3-、I-、Na+,Fe3+可以大量共存 |
| C、硝酸铵溶液不能与镁反应生成氢气而氯化铵溶液能与镁反应生成氢气 |
| D、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
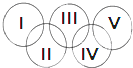 如右图,假定五环中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )
如右图,假定五环中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | |
| A | SiO2 | NaOH溶液 | CuSO4溶液 | Ag | O2 |
| B | O2 | Fe | 稀H2SO4 | NaOH溶液 | CO2 |
| C | O2 | NH3 | 稀H2SO4 | NaOH溶液 | Al |
| D | Mg | Al | CO2 | Fe2O3 | KOH溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从碘水中提取碘单质,可选用酒精作有机萃取剂 |
| B、蒸馏操作时,应使温度计的水银球深入液体中 |
| C、与盐酸反应生成CO2,碳酸钠比碳酸氢钠快 |
| D、向Na2CO3和NaHCO3溶液中分别滴加酚酞试液,两者都显红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、11.52 |
| B、11.70 |
| C、11.82 |
| D、12.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com