
| A. | ①②③⑤ | B. | ①③④ | C. | ①③⑤ | D. | ①②③④⑤ |
分析 ①硅与氯气反应生成氯化硅,氯化硅与氢气发生氧化还原反应生成硅和氯化氢;
②硫与氧气反应得到二氧化硫;
③氧化铜与盐酸反应生成氯化铜,电解氯化铜溶液得到铜和氯气;
④氯化铝为强酸弱碱盐,水溶液存在水解平衡,氯化铝溶液蒸干时,氯化氢挥发促进氯化铝的水解生成氢氧化铝;
⑤硝酸银溶液中逐滴加入氨水,先生成沉淀,继续滴加生成银氨络合溶液,银氨络合溶液与葡萄糖发生氧化还原反应生成银.
解答 解:①Si可与氯气在高温下反应生成SiCl4,SiCl4可与氢气发生反应生成Si和HCl,该反应可用于工业提纯硅,粗硅$→_{高温}^{Cl_{2}}$SiCl4$→_{高温}^{H_{2}}$Si,各步反应均能够一步实现,故正确;
②硫与氧气反应得到二氧化硫,得不到三氧化硫,故错误;
③氧化铜与盐酸反应生成氯化铜,电解氯化铜溶液得到铜和氯气,CuO$\stackrel{盐酸}{→}$CuCl2(aq)$\stackrel{电解}{→}$Cu,各步反应均能够一步实现,故正确;
④氯化铝易水解,加热溶液生成氢氧化铝和HCl,蒸发时应在HCl环境中进行,故错误;
⑤硝酸银溶液中逐滴加入氨水,先生成沉淀,继续滴加生成银氨络合溶液,银氨络合溶液与葡萄糖发生氧化还原反应生成银,AgNO3(aq)$\stackrel{NH_{3}.H_{2}O}{→}$[Ag(NH3)2]OH(aq)$→_{△}^{葡萄糖}$Ag,各步反应均能够一步实现,故正确;
故选:C.
点评 本题考查了物质的转化,注意把握物质的性质以及转化的特点、反应条件,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | HCO3-水解的离子方程式:HCO3-+H2O?CO32-+H3O+ | |
| B. | 用铜为电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2+2OH- | |
| C. | 氨水溶解氯化银固体:AgCl+2NH3•H2O═[Ag(NH3)2]++Cl-+2H2O | |
| D. | 将饱和FeCl3溶液滴入沸水中制取Fe(OH)3胶体:Fe3++3H2O?Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 英国科学家近日研发出一种名为NOTT-202a的新型多孔材料,空气中其他气体可自由通过这些空洞,但CO2会被截留.该材料的分子结构单元是以铟原子为中心,周围是以各种有机分子链条编织的“笼子”,整体上看呈现多孔特征,有些类似自然界中的蜂窝结构,下列有关说法正确的是( )
英国科学家近日研发出一种名为NOTT-202a的新型多孔材料,空气中其他气体可自由通过这些空洞,但CO2会被截留.该材料的分子结构单元是以铟原子为中心,周围是以各种有机分子链条编织的“笼子”,整体上看呈现多孔特征,有些类似自然界中的蜂窝结构,下列有关说法正确的是( )| A. | 该材料完全由金属元素构成 | |
| B. | 该材料能捕集CO2,是因为该材料可以选择性吸收CO2 | |
| C. | 该材料捕集11.2LCO2后,增重22g | |
| D. | 可利用该材料将空气中的CO2,完全捕集,从而控制温室效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对分子质量相同,结构不同的化合物互为同分异构体 | |
| B. | 同分异构体间的相互转化不存在能量的变化 | |
| C. | C4H10的一氯代物共2种结构 | |
| D. | 甲苯( )苯环上的氢原子被一个氯原子取代后的产物共有3种 )苯环上的氢原子被一个氯原子取代后的产物共有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
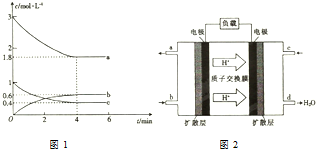 甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.
甲醇是一种低碳能源,在全球能源危机和环境污染的背景下具有良好的发展前景,在催化剂作用下可用H2(g)+CO(g)$\stackrel{催化剂}{?}$CH3OH(g),三种物质的物质的量浓度随时间变化的关系如图1所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,将1molN2和3molH2H混合,充分反应后转移电子数为6NA | |
| B. | 常温下,5.6gFe与足量浓硝酸作用转移电子数一定为0.3NA | |
| C. | 65gZn与一定量的浓硫酸反应至完全溶解,转移电子数一定为2NA | |
| D. | 6.4g由S2、S4、S8组成的混合物中含有硫原子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
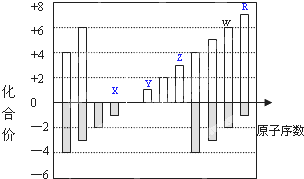 如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )| A. | Y和Z两者最高价氧化物对应的水化物能相互反应 | |
| B. | 气态氢化物的稳定性:W>R | |
| C. | WO3和水反应形成的化合物是离子化合物 | |
| D. | 原子半径:Z>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| 选项 | 气体 | 试剂 | 现象 | 结论 |
| A | X | 澄清石灰水 | 溶液变浑浊 | X一定是CO2 |
| B | Cl2 | 紫色石蕊试液 | 溶液先变红后褪色 | Cl2具有酸性和漂白性 |
| C | NO2 | KI淀粉溶液 | 溶液变为蓝色 | NO2水溶液具有氧化性 |
| D | NH3 | 酚酞试液 | 溶液变为红色 | NH3属于碱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子键就是使阴、阳离子结合成化合物的静电引力 | |
| B. | 所有金属与所有非金属原子之间都能形成离子键 | |
| C. | 配位键在形成时,由成键双方各提供一个电子形成共用电子对 | |
| D. | 金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com