
| A、品红溶液通入SO2后,红色消失 | B、显红色的酚酞溶液通入SO2后,红色褪去 | C、加有酚酞的水中投入Na2O2粉末溶液先变红,后褪色 | D、将新制氯水滴入紫色石蕊试液先变红,后褪色 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
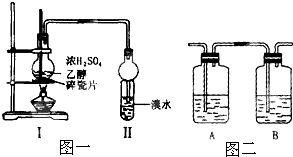
(10分)某化学兴趣小组用下图所示装置进行探究实验,以验证烧瓶中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到溴水褪色,烧瓶中浓硫酸与乙醇的混合液变为棕黑色。
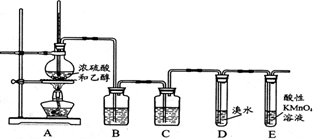
(1)烧瓶中除了浓硫酸和乙醇之外,还放入了___________,其作用是_______________
(2)写出该实验中生成乙烯的化学方程式:______________________________________
(3)B瓶中盛装的溶液是___________,其作用是 ________________________________
(4)C瓶中盛装的溶液是___________ ,其作用是_________________________________
(5)考虑到A中混合液反应的复杂性,如果没有B、C装置,D中溴水褪色的现象不能证明A的烧瓶中有乙烯生成且具有不饱和性,其理由是___________(填下列这项的序号)。
①乙烯与溴水易发生取代反应 ②使溴水褪色的反应未必是加成反应
③使溴水褪色的物质未必是乙烯 ④浓硫酸氧化乙醇生成乙醛,也会使溴水褪色
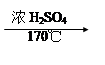 |
查看答案和解析>>
科目:高中化学 来源:2012年苏教版高中化学选修2 4.3 复合材料的制造练习卷(解析版) 题型:填空题
“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有划时代的意义。请你回答以下问题:
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
SiO2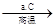 Si(粗)
Si(粗) 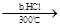 SiHCl3
SiHCl3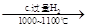 Si(纯)
Si(纯)
①写出步骤a的化学方程式_________________________________________________。
此反应不能证明C的非金属性比Si强,请你用一个化学方程式来说明C的非金属性比Si强的事实______________________________________。
②步骤b经过冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3的主要化学操作的名称是________;
(2)磁性材料。这种材料一般含有铁元素,铁以化学性质活泼用途广泛而著称。其中在工业上常用于印刷铜电路板工业,请写出反应的离子方程式_____________________________。
(3)激光材料。我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:__________________________________,________________________________。
(4)纳米材料。胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直径大约是________,区分胶体和溶液最经典的方法是___________________。
(5)高分子材料。一种新型高效净水剂[AlFe(OH)nCl6-n]m属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为________价。
查看答案和解析>>
科目:高中化学 来源:2010-2011年贵州省高二下学期期末考试 题型:实验题
(10分)某化学兴趣小组用下图所示装置进行探究实验,以验证烧瓶中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到溴水褪色,烧瓶中浓硫酸与乙醇的混合液变为棕黑色。
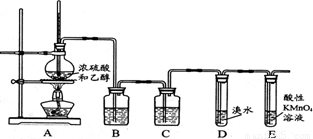
(1)烧瓶中除了浓硫酸和乙醇之外,还放入了___________,其作用是_______________
(2)写出该实验中生成乙烯的化学方程式:______________________________________
(3)B瓶中盛装的溶液是___________,其作用是 ________________________________
(4)C瓶中盛装的溶液是___________ ,其作用是_________________________________
(5)考虑到A中混合液反应的复杂性,如果没有B、C装置,D中溴水褪色的现象不能证明A的烧瓶中有乙烯生成且具有不饱和性,其理由是___________(填下列这项的序号)。
①乙烯与溴水易发生取代反应 ②使溴水褪色的反应未必是加成反应
③使溴水褪色的物质未必是乙烯 ④浓硫酸氧化乙醇生成乙醛,也会使溴水褪色
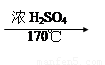 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com