
”¾ĢāÄæ”æČēĶ¼ŹĒ²æ·Ö¶ĢÖÜĘŚŌŖĖŲµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļ£Ø»ņĘäČÜŅŗ£©µÄ×Ŗ»Æ¹ŲĻµ£®ŅŃÖŖŌŚ³£ĪĀ³£Ń¹ĻĀ£¬AŹĒ¹ĢĢ壬B”¢C”¢D”¢EŹĒ·Ē½šŹōµ„ÖŹĒŅ¶¼ŹĒĘųĢ壬C³Ź»ĘĀĢÉ«£»»ÆŗĻĪļFŹĒµ»ĘÉ«¹ĢĢ壬»ÆŗĻĪļGµÄŃęÉ«·“Ó¦ĪŖ»ĘÉ«£¬»ÆŗĻĪļIŗĶJĶس£×“æöĻĀ³ŹĘųĢ¬£»DŗĶEµÄ·“Ó¦ŹĒ»Æ¹¤Éś²śÖŠµÄŅ»ÖÖÖŲŅŖµÄ¹ĢµŖ·“Ó¦£® 
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁE ŗĶJµÄµē×ÓŹ½·Ö±šŹĒŗĶ £®
¢ŚŠ“³öFŗĶCO2·“Ó¦µÄ»Æѧ·½³ĢŹ½²¢ÓƵ„ĻßĒŷرķŹ¾µē×Ó×ŖŅʵÄĒéæö
¢Ū½«ÉŁĮæµ„ÖŹCĶØČėŹ¢ÓŠµķ·Ūµā»Æ¼ŲČÜŅŗµÄŹŌ¹ÜÖŠ£¬ČÜŅŗ±äĄ¶É«£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ £®
¢Ü±źæöĻĀ3.36LĘųĢåBÓėAĶźČ«·“Ó¦£¬×ŖŅʵē×ӵďżÄæĪŖ £®
”¾“š°ø”æ![]() £»
£»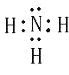 £»
£»![]() £»Cl2+2I©ØTI2+2Cl©£»1.806”Į1023
£»Cl2+2I©ØTI2+2Cl©£»1.806”Į1023
”¾½āĪö”æ½ā£ŗ»ÆŗĻĪļGµÄŃęÉ«·“Ó¦ĪŖ»ĘÉ«£¬ŗ¬ÓŠNaŌŖĖŲ£¬FÄÜÓė¶žŃõ»ÆĢ¼·“Ó¦µĆµ½ĘųĢåµ„ÖŹBÓėG£¬æÉĶĘÖŖFĪŖNa2O2 £¬ BĪŖO2 £¬ GĪŖNa2CO3 £¬ ¶ųAÓėB£ØŃõĘų£©·“Ó¦µĆµ½F£Ø¹żŃõ»ÆÄĘ£©£¬ŌņAĪŖNa£®G£ØNa2CO3£©ÓėI·“Ó¦µĆµ½CO2 £¬ ŌņIŹōÓŚĖį£¬IÓÉĘųĢå·Ē½šŹōµ„ÖŹCÓėDŌŚ¹āÕÕĢõ¼žĻĀµĆµ½£¬ŌņIĪŖHCl£¬C”¢D·Ö±šĪŖH2”¢Cl2ÖŠµÄŅ»ÖÖ£¬IŗĶJĶس£×“æöĻĀ³ŹĘųĢ¬£¬¶žÕß·“Ó¦µĆµ½ļ§ŃĪ£¬ĒŅDŗĶEµÄ·“Ó¦ŹĒ»Æ¹¤Éś²śÖŠµÄŅ»ÖÖÖŲŅŖµÄ¹ĢµŖ·“Ó¦£¬æÉĶĘÖŖJĪŖNH3 £¬ DĪŖH2 £¬ EĪŖN2 £¬ ļ§ŃĪĪŖNH4Cl£¬¹ŹCĪŖCl2 £® ¢ŁÓÉÉĻŹö·ÖĪöæÉÖŖ£¬EĪŖN2 £¬ µē×ÓŹ½ĪŖ ![]() £¬JĪŖNH3 £¬ µē×ÓŹ½ĪŖ£ŗ
£¬JĪŖNH3 £¬ µē×ÓŹ½ĪŖ£ŗ 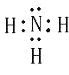 £¬ĖłŅŌ“š°øŹĒ£ŗ
£¬ĖłŅŌ“š°øŹĒ£ŗ ![]() £»
£» 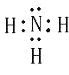 £»¢ŚNa2O2ŗĶCO2·“Ó¦µÄ»Æѧ·½³ĢŹ½²¢ÓƵ„ĻßĒŷرķŹ¾µē×Ó×ŖŅʵÄĒéæö£ŗ
£»¢ŚNa2O2ŗĶCO2·“Ó¦µÄ»Æѧ·½³ĢŹ½²¢ÓƵ„ĻßĒŷرķŹ¾µē×Ó×ŖŅʵÄĒéæö£ŗ ![]() £¬ĖłŅŌ“š°øŹĒ£ŗ
£¬ĖłŅŌ“š°øŹĒ£ŗ ![]() £»¢Ū½«ÉŁĮæµ„ÖŹCl2ĶØČėŹ¢ÓŠµķ·Ūµā»Æ¼ŲČÜŅŗµÄŹŌ¹ÜÖŠ£¬ČÜŅŗ±äĄ¶É«£¬ĖµĆ÷Éś³Éµāµ„ÖŹ£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗCl2+2I©ØTI2+2Cl© £¬ ĖłŅŌ“š°øŹĒ£ŗCl2+2I©ØTI2+2Cl©£»¢ÜAŗĶB·“Ó¦·½³ĢŹ½ĪŖ£ŗ2Na+O2
£»¢Ū½«ÉŁĮæµ„ÖŹCl2ĶØČėŹ¢ÓŠµķ·Ūµā»Æ¼ŲČÜŅŗµÄŹŌ¹ÜÖŠ£¬ČÜŅŗ±äĄ¶É«£¬ĖµĆ÷Éś³Éµāµ„ÖŹ£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗCl2+2I©ØTI2+2Cl© £¬ ĖłŅŌ“š°øŹĒ£ŗCl2+2I©ØTI2+2Cl©£»¢ÜAŗĶB·“Ó¦·½³ĢŹ½ĪŖ£ŗ2Na+O2 ![]() Na2O2 £¬ ²Ī¼Ó·“Ó¦ŃõĘųĪŖ
Na2O2 £¬ ²Ī¼Ó·“Ó¦ŃõĘųĪŖ ![]() =0.15mol£¬·“Ó¦ÖŠŃõŌŖĖŲÓÉ0¼Ū½µµĶĪŖ©1¼Ū£¬×ŖŅʵē×ӵďżÄæĪŖ0.15mol”Į2”Į6.02”Į1023mol©1=1.806”Į1023 £¬
=0.15mol£¬·“Ó¦ÖŠŃõŌŖĖŲÓÉ0¼Ū½µµĶĪŖ©1¼Ū£¬×ŖŅʵē×ӵďżÄæĪŖ0.15mol”Į2”Į6.02”Į1023mol©1=1.806”Į1023 £¬
ĖłŅŌ“š°øŹĒ£ŗ1.806”Į1023 £®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ŃŠ¾æŠ”×éĪŖĢ½¾æČõĖįŠŌĢõ¼žĻĀĢś·¢Éśµē»ÆѧøÆŹ“ĄąŠĶµÄÓ°ĻģŅņĖŲ£¬½«»ģŗĻ¾łŌȵĊĀÖĘĢś·ŪŗĶĢ¼·ŪÖĆӌ׶ŠĪĘæµ×²æ£¬ČūÉĻĘæČū(ČēĶ¼1)”£“Ó½ŗĶ·µĪ¹ÜÖŠµĪČė¼øµĪ“×ĖįČÜŅŗ£¬Ķ¬Ź±²āĮæČŻĘ÷ÖŠµÄŃ¹Ēæ±ä»Æ”£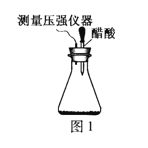
£Ø1£©ĒėĶź³ÉŅŌĻĀŹµŃéÉč¼Ę±ķ(±ķÖŠ²»ŅŖĮōæÕøń)£ŗ
±ąŗÅ | ŹµŃéÄæµÄ | Ģ¼·Ū/g | Ģś·Ū/g | “×Ėį/% |
¢Ł | ĪŖŅŌĻĀŹµŃé×÷²ĪÕÕ | 0.5 | 2.0 | 90.0 |
¢Ś | “×ĖįÅØ¶ČµÄÓ°Ļģ | 0.5 | ______ | 36.0 |
¢Ū | _________ | 0.2 | 2.0 | 90.0 |
£Ø2£©±ąŗÅ¢ŁŹµŃé²āµĆČŻĘ÷ÖŠŃ¹ĒæĖꏱ¼ä±ä»ÆČēĶ¼2”£t2Ź±£¬ČŻĘ÷ÖŠŃ¹ĒæĆ÷ĻŌŠ”ÓŚĘšŹ¼Ń¹Ē棬ĘäŌŅņŹĒĢś·¢ÉśĮĖ______øÆŹ“£¬øŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ______”£ĒėŌŚĶ¼3ÖŠÓĆ¼żĶ·±ź³ö·¢ÉśøĆøÆŹ“Ź±µē×ÓĮ÷¶Æ·½Ļņ______£»“ĖŹ±£¬Ģ¼·Ū±ķĆę·¢ÉśĮĖ______(”°Ńõ»Æ”±»ņ”°»¹Ō”±)·“Ó¦”£
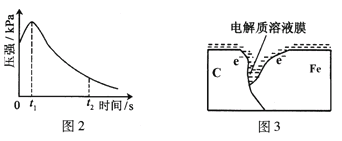
£Ø3£©øĆŠ”×é¶ŌĶ¼2ÖŠ0”«t1Ź±Ń¹Ēæ±ä“óµÄŌŅņĢį³öĮĖČēĻĀ¼ŁÉč£¬ĒėÄćĶź³É¼ŁÉ趞£ŗ
¼ŁÉčŅ»£ŗ·¢ÉśĪöĒāøÆŹ“²śÉśĮĖĘųĢ壻
¼ŁÉ趞£ŗ___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬ŗ¬ÓŠ¹²¼Ū¼üµÄĄė×Ó»ÆŗĻĪļµÄŹĒ£Ø £©
A.Na2OB.MgCl2C.Na2O2D.H2O2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚČÜŅŗÖŠÄÜ“óĮæ¹²“ęµÄĄė×Ó×éŹĒ
A£®Na+”¢OHŅ»”¢HCO3- B£®NH4+”¢NO3”Ŗ”¢OH”Ŗ
C£®H+”¢K+”¢CO32-”¢ D£®Ba2+”¢OHŅ»”¢C1”Ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·Ö×ÓÖŠĖłÓŠŌ×Ó¾łŌŚĶ¬Ņ»Ę½ĆęµÄŹĒ
A.¼×ĶéB.±½C.ŅŅ“¼D.ĘĻĢŃĢĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøßĢśĖįŃĪŌŚÄÜŌ“”¢»·±£µČ·½Ćęӊ׏ć·ŗµÄÓĆĶ¾”£ŹµŃéŹŅÓĆĀČ»ÆÄĘ”¢·ĻĢśŠ¼”¢Ļ”ĮņĖį”¢ĒāŃõ»Æ¼ŲČÜŅŗµČĪŖŌĮĻ£¬ĶعżŅŌĻĀ¹ż³ĢÖʱøøßĢśĖį¼Ų£ØK2FeO4):

(l) Na2O2µÄµē×ÓŹ½ĪŖ__________”£
(2£©²Ł×÷IµÄ²½ÖčĪŖÕō·¢ÅØĖõ”¢ĄäČ“½į¾§”¢¹żĀĖ”¢Ļ“µÓ”¢øō¾ųæÕĘų¼õŃ¹øÉŌļ.ĘäÖŠøō¾ųæÕĘų¼õŃ¹øÉŌļµÄÄæµÄŹĒ_______”£
(3£©ĘųĢåXĪŖ____£¬Š“³öFeSO4ÓėNa2O2·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ________”£
(4£©×īÖÕŌŚČÜŅŗÖŠæɵƵ½K2FeO4 ¾§ĢåµÄŌĄķŹĒ_________”£
(5£©ŅŃÖŖK2FeO4ŌŚĖ®ČÜŅŗÖŠæÉŅŌ·¢Éś£ŗ4FeO42-+10H2O![]() 4Fe(OH)3(½ŗĢå)+8OH-+3O2”ü,£¬ŌņK2FeO4 æÉŅŌŌŚĖ®“¦ĄķÖŠµÄ×÷ÓĆŹĒ__________”£
4Fe(OH)3(½ŗĢå)+8OH-+3O2”ü,£¬ŌņK2FeO4 æÉŅŌŌŚĖ®“¦ĄķÖŠµÄ×÷ÓĆŹĒ__________”£
(6£©³ĘČ”Ģį“æŗóµÄK2FeO4ѳʷ0.2100gÓŚÉÕ±ÖŠ£¬¼ÓČėĒæ¼īŠŌŃĒøõĖįŃĪČÜŅŗ£¬·“Ó¦ŗóŌŁ¼ÓĻ”ĮņĖįµ÷½ŚČÜŅŗ³ŹĒæĖįŠŌ£¬Åä³É250mL ČÜŅŗ£¬Č”³ö25.00 mL·ÅČė׶ŠĪĘ棬ÓĆ0.0l000mol/LµÄ(NH4)2Fe(SO4)2ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ÖŲø“²Ł×÷2“Ī£¬Ę½¾łĻūŗÄ(NH4)2Fe(SO4)2ČÜŅŗ30.00mL”£Éę¼°µÄÖ÷ŅŖ·“Ó¦ĪŖ:Cr(OH)4-+FeO42-=Fe(OH)3+CrO42-+OH-
Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
ŌņøĆK2FeO4ѳʷµÄ“æ¶ČĪŖ______________.
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX,Y,Z,M,N,Q½ŌĪŖ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ£¬ĘäŌ×Ó°ė¾¶ÓėÖ÷ŅŖ»ÆŗĻ¼ŪµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £© 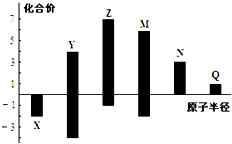
A.½šŹōŠŌ£ŗN£¾Q
B.×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĖįŠŌ£ŗM£¾Y£¾N
C.¼ņµ„Ąė×Ó°ė¾¶£ŗQ£¾N£¾X
D.Ō×ÓŠņŹż£ŗZ£¾M£¾Y£¾X
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ”°ÅØĮņĖįŹ¹ÕįĢĒĶŃĖ®”±ŹµŃéÖŠÅØĮņĖįƻӊĢåĻÖ³öµÄŠŌÖŹŹĒ£Ø £©
A.ĖįŠŌB.ĪüĖ®ŠŌC.ĶŃĖ®ŠŌD.ĒæŃõ»ÆŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. »Æѧ·“Ó¦³żĮĖÉś³ÉŠĀĪļÖŹĶā,»¹°éĖę×ÅÄÜĮæµÄ±ä»Æ
B. ·ÅČČ·“Ó¦Ņ»¶Ø²»ŠčŅŖ¼ÓČČ¼“æÉ·¢Éś
C. ŠčŅŖ¼ÓČČ²ÅÄÜ·¢ÉśµÄ»Æѧ·“Ó¦Ņ»¶ØŹĒĪüČČ·“Ó¦
D. »Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ¶¼±ķĻÖĪŖČČĮæµÄ±ä»Æ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com