
下列实验过程中,始终无明显现象的是( )
|
| A. | SO2通入新制氯水中 | B. | NH3通入AlCl3溶液中 |
|
| C. | CO2通入CaCl2溶液中 | D. | CO2通入硅酸钠溶液中 |
考点:
二氧化硫的化学性质;氨的化学性质.
专题:
元素及其化合物.
分析:
根源化学方程式判断溶液中是否有沉淀、气体、颜色变化来确定选项.
A.根据SO2能与氯气中的氯气发生氧化还原反应生成H2SO4和HCl;
B.根据NH3通入AlCl3溶液中,NH3与水反应生成一水合氨,一水合氨与AlCl3反应生成氢氧化铝白色沉淀;
C.碳酸的酸性小于盐酸;
D.CO2通入硅酸钠溶液中,CO2和硅酸钠反应生成白色的硅酸沉淀.
解答:
解:A.根据SO2能与氯气中的氯气发生氧化还原反应生成H2SO4和HCl,氯水由黄绿色变为无色,现象明显,故A错误;
B.NH3通入AlCl3溶液中,NH3与水反应生成一水合氨,一水合氨与AlCl3反应生成氢氧化铝白色沉淀,现象明显,故B错误;
C.碳酸的酸性小于盐酸的酸性,无法和氯化钙反应,无明显现象,故C正确;
D.CO2通入硅酸钠溶液中,CO2和硅酸钠反应生成白色的硅酸沉淀,现象明显,故D错误;
故选C.
点评:
本题考查化学反应发生条件及其现象,注重基础知识考查,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
分类是学习和研究化学的一种重要方法,下列分类合理的是( )
A. K2CO3和K2O都属于盐
B. KOH和Na2CO3都属于碱
C. H2SO4和HNO3都属于酸
D. Na2O和Na2SiO3都属于氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
等质量的N2和O2的体积大小为( )
|
| A. | N2的体积比O2的体积大 | B. | N2的体积比O2的体积小 |
|
| C. | N2的体积与O2的体积一样大 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
将6.50g锌投入200mL某浓度的盐酸中,锌和盐酸恰好完全反应.求:
(1)反应中生成的H2在标准状况下的体积.
(2)所用盐酸中HCl中的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述或操作不正确的是( )
|
| A. | 浓硫酸具有强氧化性,稀硫酸无氧化性 |
|
| B. | 浓硫酸不慎沾到皮肤上,立即用大量的水冲洗 |
|
| C. | 稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌 |
|
| D. | 浓硫酸与碳的反应中,浓硫酸仅表现强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
|
| A. | 活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 |
|
| B. | 同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不相等 |
|
| C. | 将SO2气体通入BaCl2溶液中至饱和,未见沉淀生成,继续通入NO2则有沉淀生成 |
|
| D. | 除FeCl2溶液中的少量FeCl3,可用加入足量铁屑过滤的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生课外活动小组利用右图所示装置分别做如下实验:
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是 溶液;加热时溶液由红色逐渐变浅的原因是: .
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是 溶液;加热时溶液由无色变为红色的原因是: .

查看答案和解析>>
科目:高中化学 来源: 题型:
某高聚物的结构片段如下:
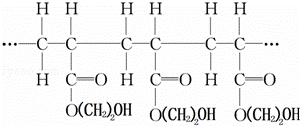
下列分析正确的是( )
|
| A. | 它是缩聚反应的产物 |
|
| B. | 其单体是CH2=CH2COOH和HOCH2CH2OH |
|
| C. | 其链节是CH3CH2COO(CH2)2OH |
|
| D. | 其单体是CH2=CHCOO(CH2)2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合物澄清透明的水溶液中,可能含有以下离子中若干种:K+、Ca2+、Fe2+、Cu2+、Cl﹣、CO32﹣、SO42﹣,现每次取该溶液100.00mL溶液进行以下实验:
①第一份加入AgNO3溶液发现有沉淀生成;
②第二份加足量BaCl2溶液生成沉淀,洗涤后干燥得沉淀6.27g,再将该沉淀加入足量盐酸溶解后再过滤洗涤干燥得沉淀2.33g.
请回答下列问题:
(1)根据以上实验判断,原溶液中可能存在的离子是 .
(2)原溶液中一定存在的阳离子是 ,其物质的量浓度至少为 mol/l.
(3)原溶液中一定存在的阴离子是﹣ ,其物质的量浓度分别为 mol/L、 mol/l.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com