
| 应称取Na2CO3的质量 26.5(g) | 应选用容量瓶的规格 250mL(mL) | 除容量瓶外还需要的其它玻璃仪器是上图中的烧杯、胶头滴管及玻璃棒 |
分析 (1)根据m=nM=cVM求出溶质质量,容量瓶没有200mL;操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作确定仪器,据此解答;
(2)根据配制溶液的实验操作过程进行实验步骤排序;
(3)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=$\frac{n}{V}$分析对所配溶液浓度的影响.
解答 解:(1)容量瓶没有200mL,只能选用250mL,需碳酸钠的质量为m=0.25L×1mol•L-1×106g/mol=26.5g;
操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,故需要的仪器有:托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙,故还需玻璃仪器有:烧杯、玻璃棒、胶头滴管,
故答案为:26.5;250mL;烧杯、胶头滴管;
(2)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解,冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,故正确的操作顺序为:BACFDE;
故答案为:BACFDE;
(3)未洗涤烧杯、玻璃棒,少量碳酸钠沾在烧杯壁与玻璃棒上,碳酸钠的实际质量减小,所配溶液浓度偏低;
配制溶液时,容量瓶未干燥,溶液的体积不变,所配溶液浓度无影响;
定容时,俯视刻度线,导致溶液体积偏小,所配溶液浓度偏高,
故答案为:偏低;无影响;偏高.
点评 本题主要考查一定物质的量浓度溶液的配制、误差分析,明确配制原理和配制过程是解题关键,题目难度不大.


 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源:2016-2017学年陕西省高一上第一次月考化学卷(解析版) 题型:选择题
下列说法中不正确的是
A.物质的量是一个物理量,物质的量的单位是摩尔
B.2 mol水的摩尔质量是1 mol水的摩尔质量的2倍
C.N2、CO组成的混合气体28g,其物质的量为1mol
D.标准状况下, 2L二氧化碳和3L一氧化碳所含有的原子数目相等.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锥形瓶洗净后还留有蒸馏水 | |
| B. | 取碱液的滴定管开始有气泡,放出液体后气泡消失 | |
| C. | 溶液颜色较浅时滴入酸液过快,停止滴定后反加一滴NaOH溶液无变化 | |
| D. | 用碱式滴定管取一定体积的NaOH溶液时,量取前仰视读数,量取后俯视读数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应A(g)?2B(g)△H,若正反应的活化能为Ea kJ•mo-l,逆反应的活化能为Eb kJ•mol-l,则△H=-( Ea-Eb)kJ.mol-l | |
| B. | 某温度下,氯化钠在水中的溶解度是20 g,则该温度下的饱和氯化钠溶液溶质的质量分数为20% | |
| C. | 将0.2 mol•L-1的CH3COOH溶液与0.1 mol•L-1的NaOH溶液等体积混合后,溶液中有关粒子的浓度满足下列关系:2c(H+)-c(OH-)=c(CH3COO-)-c(CH3COOH) | |
| D. | 将浓度为0.1 mol•L-1 HF溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变,$\frac{c({F}^{-})}{c({H}^{+})}$始终保持增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “沙尘暴”属于一种自然现象,与人类活动无关 | |
| B. | 碳酸铝是一种应用很广的视频添加剂,可大量添加到馒头、面包、油条等食品中 | |
| C. | 利用垃圾发电能达到节能减排的目的 | |
| D. | 持续高温天气的出现与人类活动无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和氯气混合后光照发生反应 | B. | 乙炔和氯气的加成反应 | ||
| C. | 甲苯与等物质的量的Br2发生反应 | D. | 乙烯与水的加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
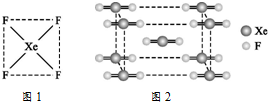 自从英国化学家巴特列(N.Bartlett)首次合成了第一种稀有气体的化合物XePtF6以来,人们又相继发现了氙的一系列化合物,如XeF2、XeF4等.巴特列为开拓稀有气体化学作出了历史性贡献.
自从英国化学家巴特列(N.Bartlett)首次合成了第一种稀有气体的化合物XePtF6以来,人们又相继发现了氙的一系列化合物,如XeF2、XeF4等.巴特列为开拓稀有气体化学作出了历史性贡献.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com