���
�⣺4NH
3+5O
24NO+6H
2O�����а��Ĵ�����ʵ�飬�谱����������������̼������Ʊ��������ö�����̼��������Ʒ�Ӧ�Ʊ����������������������ò�����������һ�����������������ǿ�����Ⱦ����������β�����գ�
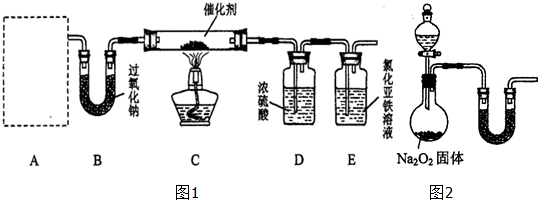
��1������A��ʹ�õ�ҩƷ��NH
4HCO
3���壬����NH
4HCO
3������Ҫ�ƾ��ƣ��ʴ�Ϊ���ƾ��ƣ�
��װ��B��ʢ�Ź������ƣ�̼����泥����ȷֽ�����NH
3��CO
2��H
2O���������ƺ�ˮ��Ӧ2Na
2O
2+2H
2O=4NaOH+O
2�����÷�Ӧ���ṩ������������̼��������ƣ�2Na
2O
2+2CO
2�T2Na
2CO
3+O
2���÷�ӦҲ���ṩ����������װ��B����������ˮ�Ͷ�����̼��Ӧ������C������ķ�Ӧ��������
�ʴ�Ϊ����ˮ�Ͷ�����̼��Ӧ������C������ķ�Ӧ��������
��NH
3�����O
2�ڴ��������������·�����Ӧ����һ��������ˮ����Ӧ����Ϊ��4NH
3+5O
24NO+6H
2O��
�ʴ�Ϊ��4NH
3+5O
24NO+6H
2O��
����A��B��ҩƷ������������Ȼ�������Һ������Ϊһ�������������Ļ�����壬4NO+3O
2+2H
2O=4HNO
3�������ܽ��������������������ӣ�������Һ��Ϊ��ɫ��
�ʴ�Ϊ����Һ��Ϊ��ɫ��
��Ϊ��ֹ����������װ��C��D֮������һ��������װ�ã�һ�������Լ����ɵĶ����������ж���Ӧ��һ��β������װ�ã�
�ʴ�Ϊ��D��Һ����ܻᵹ����β������Ⱦ������
����A�й�������������7.9g����μӷ�Ӧ��NH
4HCO
3����Ϊ
=0.1mol��NH
4HCO
3NH
3��+H
2O+CO
2�������ɰ�����������̼��ˮ��0.1mol��������������Ʋ���Ӧ��������̼��ˮ��������Ʒ�Ӧ��0.1mol��������0.5mol������������������ʵ���Ϊ0.1mol+0.05mol+0.05mol=0.2mol��V=nV
m=0.2mol��22.4mol/L=4.48L��
�ʴ�Ϊ��4.48��
��2��Aװ���ṩ������̼��ˮ������������װ��BΪ���ﰱ�������Ե��й������ƴ���ʱ����Ũ��ˮ��ʡ���˽�������̼��ˮ����ת��������������Ϊ�������壬���ﰱ��������ӦΪ���Ի�������ѡ�ü�ʯ�ң����������ơ������ƣ���
�ʴ�Ϊ��Ũ��ˮ����ʯ�ң����������ơ������ƣ���




 ���Ṥҵ��SO2��ȡSO3�ķ�ӦΪ��2SO2��g��+O2��g��
���Ṥҵ��SO2��ȡSO3�ķ�ӦΪ��2SO2��g��+O2��g��