
| A. | 等于5 s | B. | 大于5 s | C. | 等于10 s | D. | 小于5 s |
分析 c(HI)由0.1mol/L降到0.07mol/L需要15s,则v(HI)=$\frac{0.1mol/L-0.07mol/L}{15s}$=0.002mol/(L.s),化学反应速率与反应物浓度成正比,反应物浓度越大其反应速率越快,随着反应进行反应物浓度降低,则其反应速率降低,据此分析解答.
解答 解:c(HI)由0.1mol/L降到0.07mol/L需要15s,则v(HI)=$\frac{0.1mol/L-0.07mol/L}{15s}$=0.002mol/(L.s),化学反应速率与反应物浓度成正比,反应物浓度越大其反应速率越快,随着反应进行反应物浓度降低,则其反应速率降低,c(HI)由0.07mol/L降到0.06mol/L如果反应速率为0.002mol/(L.s),则所需时间=$\frac{0.07mol/L-0.06mol/L}{0.002mol/(L.s)}$=5s,实际上反应速率小于0.002mol/(L.s),则所需时间大于5s,故选B.
点评 本题考查化学反应速率有关计算,为高频考点,明确物质浓度与反应速率关系是解本题关键,侧重考查学生分析计算能力,题目难度不大.


科目:高中化学 来源: 题型:选择题
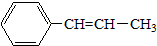 )的叙述正确的是( )
)的叙述正确的是( )| A. | 最多有5个碳原子在一条直线上 | |
| B. | 发生加聚反应的产物为: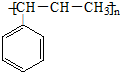 | |
| C. | 所有碳原子可能在同一平面上 | |
| D. | 1 mol该物质最多能与3 mol H2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4是酸,因为H2SO4中含有氢元素 | |
| B. | 豆浆是胶体,因为其分散质粒子直径在>1nm | |
| C. | 分子、原子、电子、质子、沙子中,沙子不适宜用物质的量描述,因为其是微观微粒 | |
| D. | 氧化铝是碱性氧化物,因为铝是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,3.2g O2和3.2g O3所含氧原子数都是0.2NA | |
| B. | 常温下,0.1mol•L-1NH4NO3溶液中,含有的氮原子数是0.2NA | |
| C. | 0.1molN2与足量的H2反应,转移的电子数是0.6NA | |
| D. | 2.24LCO和CO2的混合气体中所含的碳原子数一定是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol | B. | 0.05mol | C. | 0.15mol | D. | 0.11mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容量瓶中原有少量蒸馏水 | |
| B. | 洗涤烧杯和玻璃棒的洗涤液未转入容量瓶中 | |
| C. | 往烧杯中转移溶液时有少量液体溅出 | |
| D. | 定容时俯视 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验内容 | 实验目的 |
| A | 在碘水中加入约1mL四氯化碳,振荡试管,观察碘被四氯化碳萃取,再向试管里加入1mL浓KI水溶液,振荡试管,溶液紫色变浅 | 证明物质的溶解性规律--“相似相溶” |
| B | 取两只试管,分别加入4mL0.01mol/L KMnO4酸性溶液,然后向一只试管中加入0.1mol/LH2C2O4溶液2mL,向另一只试管中加入0.1mol/LH2C2O4溶液4mL,记录褪色时间 | 证明草酸浓度越大反应速率越快 |
| C | 分别向2mL甲苯、2mL苯、2mL正己烷中加入3滴酸性高锰酸钾溶液,振荡.甲苯中酸性高锰酸钾溶液褪色,而苯、正己烷中酸性高锰酸钾溶液不褪色 | 证明与苯环相连的甲基易被氧化 |
| D | 将反应产生的气体依次通入盛有NaOH溶液、品红溶液及酸性KMnO4溶液的试管,品红不褪色,酸性KMnO4溶液褪色 | 证明乙醇与浓硫酸混合加热可得乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | H2 | CO2 | CH3 OH | H2 O |
| 浓度(mol/L) | 0.2 | 0.2 | 0.4 | 0.4 |
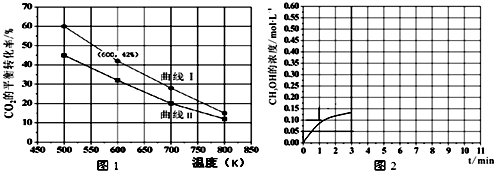
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com