
分析 (1)若氧化物X既能与某些酸性氧化物反应,又能与某些碱性氧化物反应,但反应产物中均无盐生成,则X为H2O,与氧化钠反应生成氢氧化钠;
(2)若氧化物X中氧的质量分数为47.06%,且它既能与强酸反应,又能与强碱反应,且都能生成盐和水,判断X为Al2O3,电解熔融氧化铝得到Al与氧气,则所得二价能源物质为Al;
(3)Al与氧化铁在高温条件下反应生成氧化铝与Fe,反应放出大量的热;
(4)发生反应:2Al+2H2O+2NaOH=2NaAlO2+3H2↑,生成气体为氢气,根据方程式计算混合物中Al的质量,进而计算氧化铁的质量.
解答 解:(1)若氧化物X既能与某些酸性氧化物反应,又能与某些碱性氧化物反应,但反应产物中均无盐生成,则X为H2O,与氧化钠反应生成氢氧化钠,反应方程式为:Na2O+H2O=2NaOH,
故答案为:H2O;Na2O+H2O=2NaOH;
(2)若氧化物X中氧的质量分数为47.06%,且它既能与强酸反应,又能与强碱反应,且都能生成盐和水,判断X为Al2O3,熔融Al2O3与Na2O反应的化学方程式为:Al2O3(熔融)+Na2O=2NaAlO2;电解熔融氧化铝得到Al与氧气,则所得二价能源物质为Al,
故答案为:Al2O3;Al2O3(熔融)+Na2O=2NaAlO2;Al;
(3)Al与氧化铁在高温条件下反应生成氧化铝与Fe,反应方程式为:Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+Fe,反应放出大量的热,属于放热反应,
故答案为:Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+Fe;放热;
(4)发生反应:2Al+2H2O+2NaOH=2NaAlO2+3H2↑,生成气体为氢气,氢气物质的量为$\frac{bL}{22.4L/mol}$=$\frac{b}{22.4}$mol,故Al的物质的量为$\frac{b}{22.4}$mol×$\frac{2}{3}$,Al的质量为$\frac{b}{22.4}$mol×$\frac{2}{3}$×27g/mol=$\frac{9b}{11.2}$g,混合物中氧化铁的质量是(a-$\frac{9b}{11.2}$)g,
故答案为:(a-$\frac{9b}{11.2}$)g.
点评 本题考查无机物推断,基本属于猜测验证型题目,需要学生熟练掌握元素化合物知识,难度较大.


科目:高中化学 来源: 题型:选择题
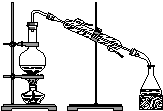 | 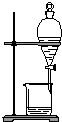 |  | 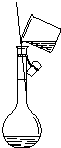 |
| A用海水制蒸馏水 | B将碘水中的碘单质与水直接分离 | C除去Fe(OH)3胶体中的FeCl3 | D稀释浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合金都一定是两种金属熔合而成 | |
| B. | 涂料属于高分子材料,不属于合成材料 | |
| C. | 水泥与水搅拌静之后会凝固变硬,这是水泥的水硬性 | |
| D. | 我国的陶都和瓷都都是宜兴 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
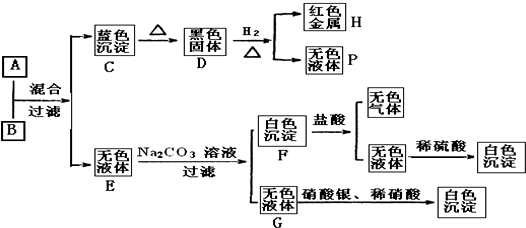
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | M可能为铜,X可能为氯化铁 | B. | M可能为石墨,Y可能为硫酸铁 | ||
| C. | 电子由铁经盐桥流向M极 | D. | 盐桥中K+向铁极迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  用如图所示装置,制备并收集少量NO2气体 | |
| B. |  用如图所示装置,除去CO2中的HCl | |
| C. |  用图所示装置,制备Fe(OH)2并能较长时间观察其颜色 | |
| D. |  用图所示装置,所示装置制取并收集干燥纯净的NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使甲基橙变红的溶液中:NH4+、Mg2+、SO42-、NO3- | |
| B. | 1.0 mol•L-1FeCl3溶液:Na+、Cl-、NO3-、SCN- | |
| C. | 1.0 mol•L-1的KNO3溶液中:Fe2+、H+、Cl-、SO42- | |
| D. | 与Al反应能放出H2的溶液中:Na+、Cl-、HCO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
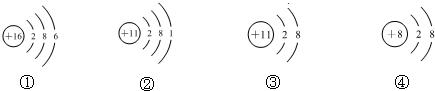
| A. | 它们表示四种元素 | |
| B. | ②③的化学性质相同 | |
| C. | ②表示的元素是金属元素 | |
| D. | ①表示的是原子,而④表示的是阴离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com