
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
分析 分子式为C4H8且含一个支链的链状有机物为CH2=C(CH3)2,先根据等效氢找一氯代物,CH2=C(CH3)2共有2种一氯代物,然后一氯代物中氢原子的种类可得二氯代物的种类.
解答 解:分子式为C4H8且含一个支链的链状有机物为CH2=C(CH3)2,CH2=C(CH3)2共有2种一氯代物,二氯代物有4种:CCl2=C(CH3)2,CHCl=C(CH2Cl)CH3,CH2=C(CHCl2)CH3,CH2=C(CHCl2)CH3,CH2=C(CH2Cl)2,故选A.
点评 本题难度较大,侧重对学生能力的培养,做题注意先判断该有机物中有几个等效氢原子,先固定一个氯原子的位置(生成一个一氯代物),然后对其二氯代物可能的情况进行书写.


科目:高中化学 来源: 题型:选择题
| A. | NaHSO4═Na++HSO4- | B. | NaHCO3═Na++H++CO32- | ||
| C. | KClO3═K++Cl-+3O2- | D. | Al2(SO4)3═2Al3++3SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱:苛性碱、纯碱、火碱 | |
| B. | 碱性氧化物:氧化铜、氧化铁、七氧化二锰、二氧化硅 | |
| C. | 混合物:水煤气、矿泉水、盐酸 | |
| D. | 无丁达尔现象的分散系:氯化铁溶液、碘的四氯化碳溶液、蒸馏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:X2->Y->Z2+ | |
| B. | 单质的熔点:Z>W>Y | |
| C. | 能破坏水的电离平衡的离子为:Y-,Z2+,W- | |
| D. | 离子化合物ZX的熔点高,ZX可作为耐火材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和CH3-CH2-CH3 | B. | C2H5-OH和C6H5-OH | ||
| C. | CH3-CH2-CH2-CH3和 | D. | C2H4和C3H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 、I
、I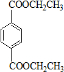 .
.
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com