
(4分) 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O △H2= -534.2kJ·mol-1
写出肼和N2O4 反应的热化学方程式 ;
(1)2NH3+NaClO==N2H4+NaCl+H2O
(2)2N2H4 (1)+N2O4(1)==3N2(g)+4H2O(g) △H= -1048.9kJ·mol-1
【解析】(1)NH3+NaClO——N2H4,根据元素守恒还应生成NaCl和H2O,观察法可配平方程式为 2NH3+NaClO==N2H4+NaCl+H2O;
(2)肼与N2O4反应生成N2和水蒸气:2N2H4 +N2O4==3N2+4H2O;
观察已知的两个热方程式可知,②×2-①得:
2N2H4 (1)+N2O4(1)==3N2(g)+4H2O(g) △H=△H2×2-△H1="=" -1048.9kJ·mol-1


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源:2013届江西省上饶市横峰中学高三第一次月考化学试卷(带解析) 题型:填空题
(本题共12分)
Ⅰ、氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)氮元素原子的L层电子数为 ;
(2) NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g) = N2O4(l) ΔH1=-19.5kJ?mol-1
②N2H4(l) + O2 (g)=N2(g)+2H2O(g) ΔH2 ="-534.2" kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为 。
Ⅱ、一定质量的液态化合物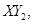 在标准状况下的一定质量的
在标准状况下的一定质量的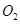 中恰好完全燃烧,反应方程式为:
中恰好完全燃烧,反应方程式为: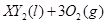 ===
===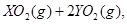 冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56
冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56 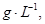 则:
则:
(1)反应前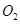 的体积是 。 (2)化合物
的体积是 。 (2)化合物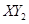 的摩尔质量是 。
的摩尔质量是 。
(3)若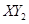 分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为 和 (写元素符号)。
分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为 和 (写元素符号)。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年安徽省铜陵一中高二10月月考化学试卷(带解析) 题型:填空题
(4分) 氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -195kJ·mol-1
②N2H4 (1) + O2(g)= N2(g) + 2 H2O △H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江西省上饶市高三第一次月考化学试卷(解析版) 题型:填空题
(本题共12分)
Ⅰ、氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用。回答下列问题:
(1)氮元素原子的L层电子数为 ;
(2) NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为 ;
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g) = N2O4(l) ΔH1=-19.5kJ∙mol-1
②N2H4(l) + O2 (g)=N2(g)+2H2O(g) ΔH2 =-534.2 kJ·mol-1
写出肼和N2O4反应的热化学方程式 ;
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的反应式为 。
Ⅱ、一定质量的液态化合物 在标准状况下的一定质量的
在标准状况下的一定质量的 中恰好完全燃烧,反应方程式为:
中恰好完全燃烧,反应方程式为: 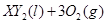 ===
===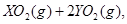 冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56
冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56  则:
则:
(1)反应前 的体积是
。
(2)化合物
的体积是
。
(2)化合物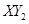 的摩尔质量是
。
的摩尔质量是
。
(3)若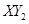 分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为
和
(写元素符号)。
分子中X、Y两元素的质量比是3∶16,则X、Y两元素分别为
和
(写元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
(13分)氮及其化合物在生产、生活和科技等方面有重要的应用,请回答下列问题:
(1)氮元素基态原子的价电子排布式为 ;
(2)在氮气分子中,氮原子之间存在着 个![]() 键和 个
键和 个![]() 键;
键;
(3)磷、氮、氧是周期表中相邻的三种元素,比较:(均填“大于”、“小于”或“等于”)
①氮原子的第一电离能 氧原子的第一电离能;
②N2分子中氮氮键的键长 白磷分子中磷磷键的键长;
(4)氮元素的氢化物(NH3)是一种易液化的气体,请阐述其原因是 ;
(5)配合物[Cu(NH3)4]Cl2中含有4个配位键,若用2个N2H4代替其中的2个NH3,得到的配合物[Cu(NH3)2(N2H4)2]Cl2中含有配位键的个数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com