
| A. | 在CH2=CH2分子中,存在4个σ键和一个π键 | |
| B. | NH3、CO、CS2都是极性分子 | |
| C. | N、O、F电负性大小:F>O>N;第一电离能大小:N>F>O | |
| D. | H2O的沸点比HF的沸点高,是由于水中氢键键能大 |
分析 A.共价单键是σ 键,共价双键中一个是σ 键一个是π键;
B、CS2是极性键形成的非极性分子;
C、得电子能力越强,电负性越大;同周期第一电离能变大,但第ⅡA、ⅤA比相邻两个都要大;
D、HF分子间形成的氢键数目比水分子间氢键数目少,所以HF的沸点比水低.
解答 解:A.共价单键是σ 键,共价双键中一个是σ 键一个是π键,所以CH2=CH2中有5个σ 键,1个π 键,故A错误;
B、CS2是极性键形成的非极性分子,氨气是极性分子,故B错误;
C、得电子能力F>O>N,所以电负性是:F>O>N;同周期第一电离能变大,但第ⅡA、ⅤA比相邻两个都要大,则第一电离能大小:N>F>O,故C正确;
D、HF分子间形成的氢键数目比水分子间氢键数目少,所以HF的沸点比水低,而不是氢键的键能大,故D错误;
故选C.
点评 本题考查了共价键的类型、极性键和非极性键的判断和氢键等知识点,利用知识迁移的方法进行分析解答,难度不大.


科目:高中化学 来源: 题型:多选题
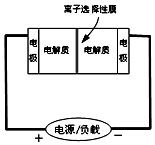 如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr下列关于此电池说法正确的是( )
如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr下列关于此电池说法正确的是( )| A. | 放电过程中钠离子从左到右通过离子交换膜 | |
| B. | 电池充电时,阴极反应为:3NaBr+2e-=NaBr3+2Na+ | |
| C. | 电池中右侧的电解质溶液为Na2S2-Na2S4混合溶液 | |
| D. | 充电的过程中当0.1molNa+通过离子交换膜时,导线通过0.1mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 500 mL 0.1 mol/L盐酸中,含有HCl分子数目为0.05NA | |
| B. | 0℃、1个标准状况下,22.4LNO和22.4LO2混合后所得气体中分子总数为1.5NA | |
| C. | 常温下.0.5 moll•L-l Fe3(SO4)2溶液中含 Fe3+数目为1NA | |
| D. | 在标准状况下,22.4 LCH4与18 g H2O所含有的质子数、电子数均为10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和稀硫酸反应:Fe+2H+═3Fe2++H2↑ | |
| B. | 硫酸铜溶液中加入氢氧化钠溶液:Cu2++2OH-═Cu(OH)2↓ | |
| C. | 实验室制取二氧化碳:CO32-+2H+═CO2↑+H2O | |
| D. | 氢氧化钡溶液和稀硫酸反应:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高纯度的单质硅可用于制作计算机芯片 | |
| B. | 钠钾合金可在快中子反应堆中作热交换剂 | |
| C. | 二氧化硫不可用作熏蒸粉丝 | |
| D. | 碳酸钠可用于治疗胃酸过多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼铜时,将粗铜与电源的负极相连 | |
| B. | 当反应物的总能量高于生成物的总能量时,该反应为吸热反应 | |
| C. | FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq)体系中加入KCl固体,平衡向逆反应方向移动 | |
| D. | 1807年,化学家戴维电解熔融氯化钾得到钾,直到现在,工业上依然用电解法制备金属钠、镁、铝等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15N与14N互为同位素 | B. | 13C与14C互为同素异形体 | ||
| C. | 13C与15N具有相同的中子数 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在7.8gNa2O2固体中,含有阴、阳离子的总数为0.3NA | |
| B. | 光照下,将16gCH4和71gCl2组成的混合气体充分反应,生成CH3Cl分子数为NA | |
| C. | 若发生水解的Fe3+为1mol,此时生成的氢氧化铁胶粒数为NA | |
| D. | 100g质量分数为46%的乙醇水溶液中,所含氢氢原子总数为6NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com