
��֪��
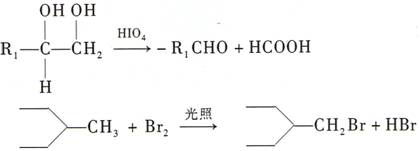
A��G�����ʼ��������ͼ��ʾ��ת����ϵ�������л���B��ʽ����̼��С16��G �ķ���ʽC8H6O4��G�ķ����к�һ�������ұ�����һ�ȴ���ֻ�����֣�1 mol ��G ������NaHCO3����Һ��Ӧ�ܲ���2 mol CO2��
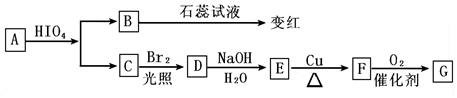
��ش��������⣺
(1)�л���B�ɷ����ķ�Ӧ������________________________��
A.������Ӧ B.�кͷ�Ӧ C.������Ӧ D.�ӳɷ�Ӧ
��д���л���Ľṹ��ʽ��A________________________��C________________ ��
(3)�л���E�ķ�������ͬ���칹���кܶ࣬��������FeCl3��Һ������ɫ��Ӧ���ұ�����һ�ȴ�����4 ��ͬ���칹��Ľṹ��ʽΪ(д��4 ��)��
________________��________________��________________��________________________��
��4��д����Ӧ�Ļ�ѧ����ʽ��ָ����Ӧ�����͡�
D �� E_______________________________________________________________
F �� G___________________________________________________________________
 ��Ԫȫ��������ϵ�д�
��Ԫȫ��������ϵ�д� �»ƸԱ����ܾ�ϵ�д�
�»ƸԱ����ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


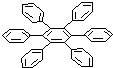

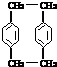

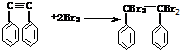
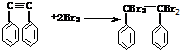
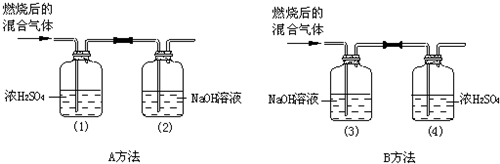
| ȼ���л�������� | ʵ�鷽�� | ʵ��ǰ���-��װ������ | |||
| ʵ��ǰ | ʵ��� | ||||
| ���� | 5.4g | A | ��150g | ��153.6g | |
| ��150g | ��165.4g | ||||
| ���� | 5.4g | B | ��150g | ��166.0g | |
| ��150g | ��154.2g | ||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| 3 |
| 2 |
| 3 |
| 2 |
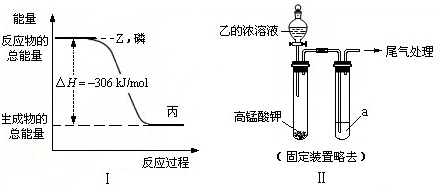
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012�����������������ѧ��һ��ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
��10�֣��Իش����и����⣺
��1����ͼ����ʾ��1 mol NO2��CO��Ӧ���� CO2��NO�����������仯ʾ��ͼ����д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ�� ��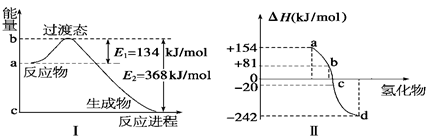
��2����ѧ��Ӧ���ʱ��뷴Ӧ���������ļ����йء�
����֪��H2(g)+Cl2(g) ="==" 2HCl(g) ��H="-185" kJ/mol;
���ܦ�H298(H��H)="436" kJ/mol,��H298(Cl��Cl)="247" kJ/mol,��H298(H��Cl)= ��
��ͼ���ʾ����Ԫ���е���������(Se)���������⻯��ʱ���ʱ����ݣ����������ʱ����ݿ�ȷ��a��b��c��d�ֱ������Ԫ�أ���д�������ⷢ���ֽⷴӦ���Ȼ�ѧ����ʽ�� ��
��3����֪�� ��Fe2O3(s)+3CO(g)  2Fe(s)+3CO2(g) ��H="-a" kJ/mol
2Fe(s)+3CO2(g) ��H="-a" kJ/mol
��3Fe2O3(s)+CO(g)  2Fe3O4(s)+CO2(g) ��H="-b" kJ/mol
2Fe3O4(s)+CO2(g) ��H="-b" kJ/mol
��Fe3O4(s)+CO(g)  3FeO(s)+CO2(g) ��H="+ckJ/mol"
3FeO(s)+CO2(g) ��H="+ckJ/mol"
��FeO(s) +CO(g)  Fe(s)+CO2(g) ��H=- ��
Fe(s)+CO2(g) ��H=- ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ��ӱ�ʡ������ѧ�ڵ����ο��Ի�ѧ�Ծ� ���ͣ������
X��Y��ZΪ��ͬ�����ڷǽ���Ԫ�ص���̬���ʡ���һ���������ܷ������·�Ӧ��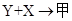 (g)��
(g)��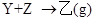 ���ס��ҿɻ����������ӻ��������Է�������С���ҡ�
���ס��ҿɻ����������ӻ��������Է�������С���ҡ�
��1��X�Ľṹʽ�� ��
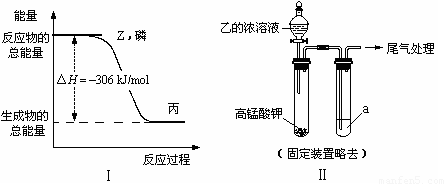
��2������Z������ȼ�տ�����Һ̬�����ӣ�Ҳ�����ɹ�̬�����ӡ���֪�������и�ԭ����������8���ӽṹ�����ĵ���ʽ�� �����ʺ�Z���ʷ�Ӧ����1 mol��ʱ����Ӧ�����������仯��ͼ����ʾ���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��3��ijͬѧ����ͼ����ʾװ��֤��������Z>I2����֪����������ҵ�Ũ��Һ��Ӧ����Z����a�� ��ˮ��Һ��������a��Ϊ��Ũ��Һ��ʵ��ʱ������������̲������嵥�����ɣ��÷�Ӧ�Ļ�ѧ����ʽ�� ��
��4����һ��Ũ�ȵ�BaCl2��Һ��ͨ��SO2���壬δ���������ɣ�����ͨ��SO2�����ͬʱ�����ɼ����е�һ�ֻ���Ԫ����ɵ�ij������������ɰ�ɫ�������ô����������________��________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com