
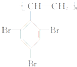
 )是性能优良的阻燃剂,其两种合成工艺如图所示.
)是性能优良的阻燃剂,其两种合成工艺如图所示.
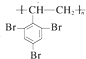 ,故C为
,故C为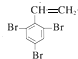 ,逆推可知B为
,逆推可知B为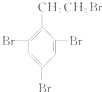 或
或 ,对应的A为
,对应的A为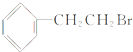 或
或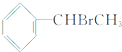 .D是高分子化合物,由转化关系可知,苯乙烯发生加聚反应生成D为
.D是高分子化合物,由转化关系可知,苯乙烯发生加聚反应生成D为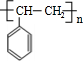 ,据此解答.
,据此解答. ,故C为
,故C为 ,逆推可知B为
,逆推可知B为 或
或 ,对应的A为
,对应的A为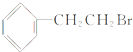 或
或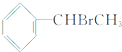 .D是高分子化合物,由转化关系可知,苯乙烯发生加聚反应生成D为
.D是高分子化合物,由转化关系可知,苯乙烯发生加聚反应生成D为 ,
, ,故答案为:
,故答案为: ;
;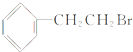 或
或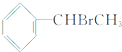 ,故答案为:
,故答案为: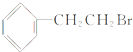 或
或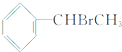 ;
; 或
或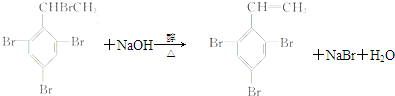 ,
, 或
或 ;
;

 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:
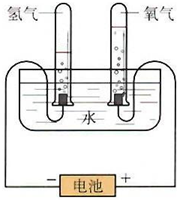 某学习小组根据图中所示的电解水原理进行实验,并对实验得到的与查阅资料获得的数据进行处理、分析,请与他们一起进行探究.请按要求填写.
某学习小组根据图中所示的电解水原理进行实验,并对实验得到的与查阅资料获得的数据进行处理、分析,请与他们一起进行探究.请按要求填写.| 质量g | 物质的量mol | H2 和O2物质的量的比 | |
| H2 | |||
| O2 |
| 条件 | 物质 | 1mol物质的体积 |
| 0℃101kPa | H2 | 22.3L |
| O2 | 22.4L | |
| CO2 | 22.4L | |
| 25℃101kPa | H2 | 24.4L |
| O2 | 24.5L | |
| CO2 | 24.5L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 酸\反应进程\ | 1min | 2 min | 3 min | 4 min | 5 min |
| 3.0mol/L HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
| 1.5 mol/L H2SO4 | 产生的气泡很少 | ||||
| 3.0mol/L H2SO4 | 产生的气泡很少 | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
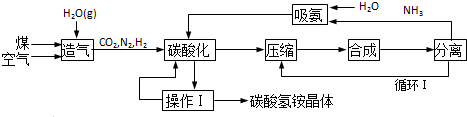
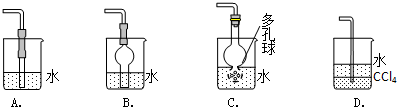
查看答案和解析>>
科目:高中化学 来源: 题型:
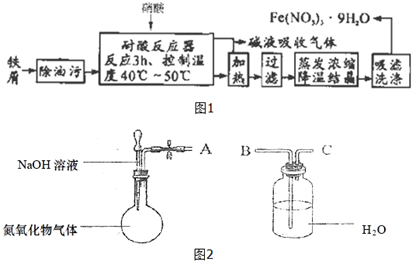
查看答案和解析>>
科目:高中化学 来源: 题型:
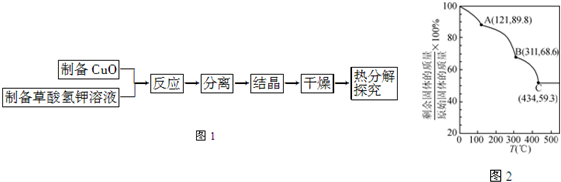
| ||
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 银盐 性质 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.34×10-6 | 7.1×10-7 | 1.1×10-8 | 6.5×10-5 | 1.0×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 今有某一种碱金属的两种碳酸盐和碱土金属(第ⅡA族)的一种不溶性碳酸盐组成的混合物,取其7.560g与过量盐酸完全反应,放出CO2体积为1.344L(标况下),另取等质量的原混合物,加水搅拌,可滤出不溶性盐1.420g.
今有某一种碱金属的两种碳酸盐和碱土金属(第ⅡA族)的一种不溶性碳酸盐组成的混合物,取其7.560g与过量盐酸完全反应,放出CO2体积为1.344L(标况下),另取等质量的原混合物,加水搅拌,可滤出不溶性盐1.420g.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com