
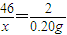 ,解得x=4.60g,
,解得x=4.60g,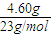 =0.2mol,n(Na2O)=
=0.2mol,n(Na2O)=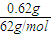 =0.01mol,
=0.01mol,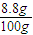 ×100%=8.8%,
×100%=8.8%,

 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
有一块表面氧化成氧化钠的金属钠,质量是5.4g,将它投入到100g水中完全反应后,收集到0.1g气体,试计算:
(1)被氧化成氧化钠的金属钠的质量是多少克?
(2)未被氧化的金属钠的质量是多少克?
(3)反应后所得溶液的溶质的质量分数是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:058
有一块表面氧化成氧化钠的金属钠,质量是5.4g,将它投入到100g水中完全反应后,收集到0.1g气体,试计算:
(1)被氧化成氧化钠的金属钠的质量是多少克?
(2)未被氧化的金属钠的质量是多少克?
(3)反应后所得溶液的溶质的质量分数是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
有一块表面氧化成氧化钠的金属钠,质量是5.4g,将它投入到100g水中完全反应后,收集到标况下1.12L的气体,试计算:
⑴未被氧化的金属钠的质量是多少克?
⑵被氧化成氧化钠的金属钠的质量是多少克?
⑶反应后所得溶液的物质的量浓度是多少?(假设溶液的体积不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com