
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向CH3CH2X中加入少量AgNO3溶液,加热 | 有浅黄色沉淀生成 | CH3CH2X中含有Br- |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热, | 没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈强碱性 |
| D | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中含有I- |
| A、A | B、B | C、C | D、D |


科目:高中化学 来源: 题型:
| A、甲基橙显黄色的溶液:AlO2-、HCO3-、Na+、K+ |
| B、c(H+)=1×10-1mol?L-1的溶液:IO3-、I-、K+、NH4+ |
| C、各离子物质的量浓度相等的溶液:K+、Na+、SO42-、NO3- |
| D、无色透明的溶液:NH4+、Na+、Cl-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中硫酸作氧化剂 |
| B、该反应显示硫酸具有酸性 |
| C、刺激性气味的气体是氨气 |
| D、NH4CuSO3中铜元素全部被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
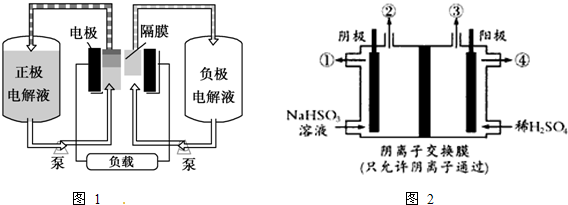
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、配制一定物质的量浓度的溶液时,容量瓶必须洁净、干燥,不漏水 |
| B、实验室里需要480 mL 2.0 mol?L-1的氢氧化钠溶液,配制溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、洗涤、定容、摇匀的步骤进行操作 |
| C、25℃时,用惰性电极电解某浓度的NaOH溶液,一小段时间后,NaOH溶液的浓度可能增大,也可能不变 |
| D、实验室配制500 mL 0.2 mol/L的硫酸亚铁溶液,其操作是:用天平称27.8 g绿矾,放入500 mL容量瓶,加水溶解、稀释、定容、摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B、用碱式滴定管量取20.00mL0.1mol/LKMnO4溶液 |
| C、向沸腾的NaOH溶液中滴加FeCl3溶液,制备Fe(OH)3胶体 |
| D、配制FeSO4溶液时,需加入少量铁粉和稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径大小:C>D>E>A |
| B、A、C的氧化物均可能含有非极性键 |
| C、B、C、D的最高价氧化物对应的水化物能两两反应 |
| D、工业中常用电解熔融DE3制备单质D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酱油 | B、面粉 | C、海带 | D、菜油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
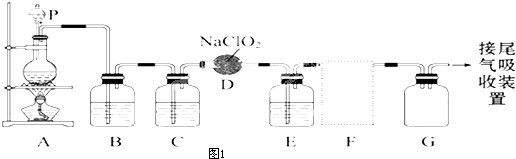
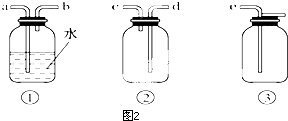
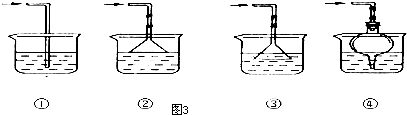
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com