

| 浓度 时间(min) 催化剂 | 30% H2O2溶液 | 15% H2O2溶液 | 5% H2O2溶液 |
| 加入WgMnO2 | 0.2 | 0.8 | 2.0 |
| 加入MgFe2O3 | 7.0 | 9.0 | 16.0 |
分析 Ⅰ(1)根据题中流程,电解硫酸氢铵水溶液得(NH4)S2O8和氢气,根据化合价升降可知,阳极的电极反应为SO42-被氧化成S2O82-;
(2)双氧水不稳定,受热容易分解,所以要得到过氧化氢溶液,就要减小压强,使液体的沸点降低;
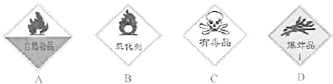
Ⅱ(1)过氧化氢是具有强氧化性的试剂,据此贴标签;
(2)根据KCN+H2O2+H2O=A+NH3↑,利用元素守恒可知生成物A的化学式;
(3)实验二:能使带火星的木条复燃的气体应为氧气;
实验三:催剂能改变化学反应速率,但自身的化学性质和质量都保持不变,据此答题;
[反思与评价]①实验三证明了氧化铁的质量不变,但要证明氧化铁是催化剂还要证明氧化铁的化学性质没有变;
②根据表中的数据可知,该对照试验比较了不同催化剂以及同一种催化剂在双氧水浓度不同时产生氧气的快慢;
解答 解:Ⅰ(1)根据题中流程,电解硫酸氢铵水溶液得(NH4)S2O8和氢气,根据化合价升降可知,阳极的电极反应为SO42-被氧化成S2O82-,阳极的电极反应方程式为2SO42--2e-=S2O82-,
故答案为:2SO42--2e-=S2O82-;
(2)双氧水不稳定,受热容易分解,所以要得到过氧化氢溶液,就要减小压强,使液体的沸点降低,
故答案为:双氧水不稳定,受热容易分解,减小压强,使液体的沸点降低;
Ⅱ(1)过氧化氢是具有强氧化性的试剂,
故选B;
(2)根据KCN+H2O2+H2O=A+NH3↑,利用元素守恒可知生成物A的化学式为KHCO3,
故答案为:KHCO3;
(3)实验二:能使带火星的木条复燃的气体应为氧气,所以可以说明氧化铁能加快氧气的产生速率,
故答案为:氧化铁能加快氧气的产生速率;
实验三:说明氧化铁在反应前后质量没有变化,
故答案为:氧化铁在反应前后质量没有变化;
[反思与评价]①实验三证明了氧化铁的质量不变,但要证明氧化铁是催化剂还要证明氧化铁的化学性质没有变,所以还需要做的实验是反应后氧化铁的化学性质没有改变,
故答案为:反应后氧化铁的化学性质没有改变;
②根据表中的数据可知,该对照试验比较了不同催化剂以及同一种催化剂在双氧水浓度不同时产生氧气的快慢,根据数据得到的结论是相同条件下,二氧化锰的催化效果比氧化铁好,其它条件相同时,双氧水的浓度越大,产生氧气的速率越快,
故答案为:相同条件下,二氧化锰的催化效果比氧化铁好,其它条件相同时,双氧水的浓度越大,产生氧气的速率越快.
点评 本题考查了电化学、实验基本操作、实验方案的设计和分析等知识,题目难度中等,试题涉及的知识点较多,充分考查了学生对所学知识的掌握情况.


科目:高中化学 来源:2016-2017学年山西省高二上10月月考化学试卷(解析版) 题型:填空题
抗酸药物的种类很多,其有效成分一般都是碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝和氢氧化镁等化学物质。
(1)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉。写出该抗酸药发挥功效时的化学方程式 、 。
(2)淀粉在抗酸药中作填充剂、黏合剂,淀粉在人体内酶的催化作用下发生水解反应,最终转化为(写分子式)_________________。
(3)服用抗酸药时,一般要嚼碎后吞服。请分析其原因:_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
下列说法中,正确的是
A.1mol任何气体的体积都是22.4L
B.1molH2的质量是1g,它所占的体积是22.4L
C.标准状况下,1molH2O所占的体积都约为22.4L
D.在标准状况下,1mol任何气体所占的体积都约为22.4L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高一阶段考一化学卷(解析版) 题型:选择题
将百分比浓度为a%,物质的量浓度为c1 mol•L﹣1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol•L﹣1,则c1和c2的数值关系是( )
mol•L﹣1,则c1和c2的数值关系是( )
A.c2=c1 B.c2<2c1 C.c2>2c1 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. |  aX(g)+bY(g)?cZ(g)密闭容器中反应达平衡,T0时条件改变如图所示,则改变的条件一定是加入催化剂 | |
| B. |  L(s)+aG(g)?bR(g)反应达到平衡时,外界条件对平衡影响如图所示,若P1>P2,则a>b | |
| C. |  aA+bB?cC物质的百分含量和温度关系如图所示,则该反应的正反应为放热反应 | |
| D. |  A+2B?2C+3D反应速率和反应条件变化关系如图所示,则该反应的正反应为放热反应,A、B、C是气体、D为固体或液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=2.5 | B. | pH=1.5 | C. | pH=12.5 | D. | pH=11.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性 | B. | 还原性 | C. | 酸性 | D. | 碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氧化剂是MnO2 还原剂是HCl | |
| B. | 每生成1 molCl2,转移电子的物质的量是2 mol | |
| C. | 每消耗1 mol MnO2,表现还原作用的HCl为4 mol | |
| D. | Cl2既是氧化产物,也是还原产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com