
����ƽ�ⳣ������Ka��ʾ)�Ĵ�С�����жϵ���ʵ����ǿ����25��ʱ���й����ʵĵ���ƽ�ⳣ�����±���ʾ��
| ��ѧʽ | HF | H2CO3 | HClO |
| ����ƽ�ⳣ�� ��Ka�� | 7.2��10��4 | K1=4.4��10��7 K2=4.7��10��11 | 3.0��10��8 |
��1�����ʵ���Ũ�Ⱦ�Ϊ0.1mol/L������������Һ�� �� Na2CO3��Һ �� NaHCO3��Һ
�� NaF��Һ �� NaClO��Һ�����������ж�pH�ɴ�С��˳���� ��
��2����Ũ��Ϊ0.1 mol/L HF��Һ��ˮϡ��һ���������¶Ȳ��䣩�����и����������____��
�� A��c(H+) B��c(H+)��c(OH��) C��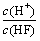 D��
D��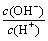
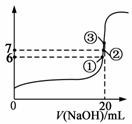 ��3��25��ʱ����20mL 0.1mol/L���������Һ�м���VmL 0.1mol/L NaOH��Һ����û����Һ��pH�仯������ͼ��ʾ������˵����ȷ���� ��
��3��25��ʱ����20mL 0.1mol/L���������Һ�м���VmL 0.1mol/L NaOH��Һ����û����Һ��pH�仯������ͼ��ʾ������˵����ȷ���� ��
A��pH��3��HF��Һ��pH��11��NaF��Һ�У�
��ˮ�������c(H+)���
B���ڢٵ�ʱpH��6����ʱ��Һ�У�
c(F��)��c(Na+) �� 9.9��10��7mol/L
C���ڢڵ�ʱ����Һ�е�c(F��) �� c(Na+)
D���ڢ۵�ʱV��20mL����ʱ��Һ��c(F��) < c(Na+)��0.1mol/L
��4����25��ʱ��Ksp[Cu(OH)2] ��2.0��10��20�� ijCuCl2��Һ��C(Cu2+)�� 0.02 mol��L��1��
���Ҫ����Cu(OH) 2������Ӧ������Һ��pHʹ֮���� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���з�Ӧ����ȡ����Ӧ����(����)
A��C2H4��3O2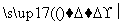 2CO2��2H2O
2CO2��2H2O
B��Zn��CuSO4===ZnSO4��Cu
C��NaCl��AgNO3===AgCl����NaNO3
D��CH2Cl2��Cl2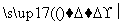 CHCl3��HCl
CHCl3��HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B��C��D���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶D>C>A>B������A��B����ͬһ���ڣ�A��C����ͬһ���塣Cԭ�Ӻ�������������A��B��ԭ�Ӻ���������֮�ͣ�Cԭ��������ϵĵ�������Dԭ��������������4�����Իش�
(1)������Ԫ�طֱ��ǣ�A________��B________��
C________��D________��
(2)������Ԫ�����ڳ��³�ѹ�µ�Һ̬����̬�⻯����ȶ����ɴ�С��˳����__________________________________________��
(3)AԪ��ij��������DԪ��ij�����ﷴӦ���ɵ��ʵĻ�ѧ����ʽ��__________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������ܴ������棬��������ӦҪ����ǣ� ��
| ѡ�� | �� �� | Ҫ �� |
| A | Na+��NO3����Cl����CH3COO�� | c��Na+���� c��NO3���� |
| B | Fe3+��NO3����Cl�� | ����KSCN��Һ����������Ѫ��ɫ���� |
| C | Na+��HCO3����Al3+��SO42�� | ��εμӰ�ˮ�����г������� |
| D | NH4+��Al3+��SO42����H+ | �μ�NaOHŨ��Һһ��ʼû��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��ѧ�о���ѧϰС����ѧϰ�ˡ���ѧ��Ӧԭ���������������µĹ����ܽᣬ������ȷ���ǣ� ��
A�������£�pH��3�Ĵ�����Һ��pH��11��NaOH��Һ�������ϣ�����
c (Na+) + c(H+) �� c(OH��) + c(CH3COO��)
B�����ѽ�����ѧƽ���ij���淴Ӧ�����ı�����ʹ��ѧƽ��������Ӧ�����ƶ�ʱ��������İٷֺ���һ�����ӡ�
C�������£�AgCl��ͬ���ʵ���Ũ�ȵ�CaCl2��NaCl��Һ�е��ܽ����ͬ
D�������£���֪�������ƽ�ⳣ��ΪKa�������ˮ��ƽ�ⳣ��ΪKh��ˮ�����ӻ�ΪKw�����У�Ka��Kh��Kw
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��д��ȷ����
A������Ͷ�뵽NaOH��Һ�У�2Al+2OH���T�T 2AlO2��+H2��
B���������ᷴӦ�� Fe + 2H+ �T�T Fe3+ + H2 ��
C����С�մ�����θ����ࣺ H+ +HCO3���T�T H2O + CO2��
D��Ba(OH)2��ϡH2SO4��Ӧ�� Ba2��+OH��+H��+SO42���T�T BaSO4��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ס�����λͬѧ��ͭ��������ԭ�ϣ������������ȡ����ͭ�ķ�����
�����٣�ͭ��Ũ�������ֱ�ӷ�Ӧ,��Cu��CuSO4
�����ڣ���Cu��CuO��CuSO4,
��ش��������⣺
��1���������١���ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ ��
�÷�Ӧ������Ũ����� �Ժ� �ԡ�
��2�������ַ���������Ϊ��һ�ַ���������? (����)��������
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪1��18��Ԫ�ص�����aW3����bX����cY2����dZ��������10�����ӣ����й�ϵ��ȷ����(����)
A����������c>b
B�������ԣ�X>W
C���⻯����ȶ��ԣ�H2Y>HZ
D��ԭ�Ӱ뾶��X<W
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ΪVa��0.05 mol·L��1 CH3COOH��Һ�м������ΪVb��0.05 mol·L��1 KOH��Һ�����й�ϵ�������(����)
A��Va>Vbʱ��c(CH3COOH)��c(CH3COO��)>c(K��)
B. Va��Vbʱ��c(CH3COOH)��c(H��)��c(OH��)
C. Va<Vbʱ��c(CH3COO��)>c(K��)>c(OH��)>c(H��)
D. Va��Vb�����ʱ��c(K��)��c(H��)��c(OH��)��c(CH3COO��)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com