
Ϊʵ��ʵ��Ŀ�ģ�ѡ�õ�װ�á�ʵ���������ȷ���ǣ� ��
ʵ��Ŀ�� | ʵ�鲽���װ�� | |
A | ̽���¶ȶԷ�Ӧ���ʵ�Ӱ�� | ��ͬ�¶��£�ȡ0.1 mol/LKI ��Һ���������ȼ��������Һ���ټ���0.1 mol/L ���ᣬ��¼��Һ������ɫ��ʱ�� |
B | ����100mL1.0mol/L NaOH��Һ | ��100mL����ƿ�м���4. 0gNaOH���壬��ˮ���̶��� |
C | ��֤�������������������� |
�����缫�����μ����軯����Һ |
D | �Ƚ�H2O2 ��Fe3+�������� | �������ữ��˫��ˮ����Fe(NO3)2��Һ�� |
A. A B. B C. C D. D
 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ��һ��ѧ�ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��0.4g NaOH��1.06g Na2CO3�ϲ������Һ������Һ�еμ�0.lmol��L��l�����ᡣ��ͼ������ȷ��ʾ������������������CO2�����ʵ����Ĺ�ϵ����
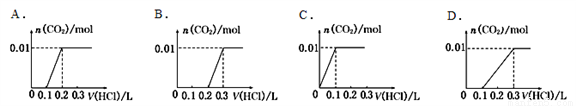
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��㶫ʡ�����и�һ��ѧ������ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A. ̼�������Һ�м�������������������Һ��Ca2����2HCO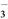 ��2OH��= CaCO3����CO
��2OH��= CaCO3����CO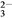 ��2H2O
��2H2O
B. �����ʯ��ˮ��ϡ���ᷴӦ��Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C. ������������Һ�е���������������Һ��Al3+ +3OH- = Al(OH)3��
D. ����CuSO4��Һ��Ӧ��2Na + Cu2+ = 2Na+ + Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ����2���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
CuI��һ�ֲ�����ˮ�İ�ɫ���壬�����ɷ�Ӧ2Cu2��+4I-=2CuI��+I2���õ�������ʯīΪ��������CuΪ�������KI��Һ��ͨ��ǰ����Һ�м���������̪�͵�����Һ����ʼ������������Һ�ʺ�ɫ������������Һ����ɫ������Щ�������ȷ������
������2I--2e-= H2����I2�����۱���
������2H2O--4e-=O2��+4H+��O2��I-����ΪI2��I2�����۱���
������2H2O+2e-= H2��+OH-��ʹc��OH-��>c��H+��
������2Cu-4e-+4I-=2CuI+I2��I2�����۱���
A. �٢� B. �٢� C. �٢� D. �ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ����2���¿������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
������̼�IJ����������������ҹ���Դ�����һ����Ҫս�Է���չ��һ����Ҫ�����˲�ҵ��
��1����֪��CH4��CO��H2��ȼ���ȷֱ�Ϊ890 kJ•mol��1��283 kJ•mol��1��285.8 kJ•mol��1���������з�Ӧ�ķ�Ӧ�ȡ�CO2��g��+CH4��g���� 2CO��g��+ 2H2��g�� ��H��____kJ•mol��1��
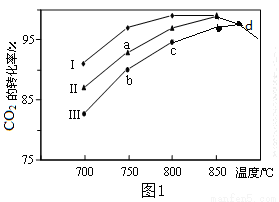
��2�����÷����е�CO2Ϊԭ����ȡ�״�����Ӧ����ʽΪ��CO2��3H2 CH3OH��H2O����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ�������������·�Ӧ��ͬʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ����ʾ��
CH3OH��H2O����������ͬ���ü״��ϳɷ�Ӧ�ڲ�ͬ�������������·�Ӧ��ͬʱ���CO2��ת�����淴Ӧ�¶ȵı仯��ͼ����ʾ��
�ٸ÷�Ӧ�Ħ�H______0�������������
��d�㲻ͬ��������������CO2��ת������ͬ��ԭ����_______________��

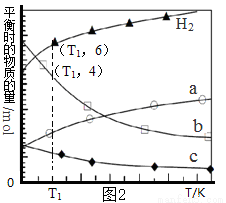
��3���ö�����̼���������ϳɵ�̼ϩ������ʼʱ��0.1MPa��n��H2����n��CO2��=3��1��Ͷ�ϱȳ��뷴Ӧ���У�������Ӧ��2CO2��g��+6H2��g�� C2H4��g��+4H2O��g����H����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ2��ʾ��
C2H4��g��+4H2O��g����H����ͬ�¶���ƽ��ʱ��������̬���ʵ����ʵ�����ͼ2��ʾ��
�ٸ÷�Ӧ��__________�Է����У�����¡����¡�����
��c������������_______________��
��T1�¶��µ�ƽ��ת����Ϊ__________________���������ʼ״̬��ƽ��ʱ�����ƽ����Է�����������İٷ���Ϊ_______________��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ѧ���ڳ����Ի�ѧ�Ծ��������棩 ���ͣ��ƶ���
�ҹ��ӹ������ijԭ�Ͼ��ⶨ��Ҫ����A��B��C��D��E����ǰ������Ԫ�أ���ԭ��������������Ԫ��A��B��C��D��E��ԭ�ӽṹ����Ϣ���£�
Ԫ�� | Ԫ�����ʻ�ԭ�ӽṹ |
A | ���ڱ���ԭ�Ӱ뾶��С��Ԫ�� |
B | ԭ�Ӻ��������ֲ�ͬ���ܼ��Ҹ����ܼ������ĵ�������ͬ |
C | �����p�������� |
D | λ�ڶ����ڣ���ԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������3�� |
E | λ�ڵ������ڣ��ڲ����ȫ��������ԭ�ӵ�������������A����ͬ |
��ش���������(��A��B��C��D��E����Ӧ��Ԫ�ط�������)��
��1��B��C��D��һ��������С����Ϊ_________________��
��2��E�Ļ�̬ԭ�ӵĺ�������Ų�ʽΪ____________��
��3��A2B2D4��������������÷�����B���ӻ���ʽΪ______________��1 mol A2B2D4�����к��ЦҼ���ĿΪ_____________��
��4���뻯����BD��Ϊ�ȵ�����������ӻ�ѧʽΪ_____________(��дһ��)��
��5��B2A6��C2A4�����о�����18�����ӣ����ǵķе����ϴ���Ҫԭ����____________��
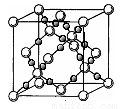
��6��BD2�ڸ��¸�ѹ�����γɾ���ľ�����ͼ��ʾ��һ���þ����к�___________��Dԭ�ӡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ������ѧ���ڳ����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£�����ָ����Һ������Ũ�ȹ�ϵ��ȷ���ǣ� ��
A. 0.1mol ��L��1NH4Cl��Һ�У�c(Cl��)>c(NH4+)>c(H+)>c(OH��)
B. 0.1mol ��L��1Na2CO3��Һ�У�c(OH��)��c(H+)+c(HCO3��)+ c(H2CO3)
C. ����ˮ�м���NaOH��Һ��pH��7��������Һ�У�c(Na+)��c(ClO��)��c(Cl��)��c(OH��)
D. 0.2mol ��L��1H2C2O4�����ᣩ��0.1mol ��L��1 NaOH��Һ�������ϵ���Һ�У�2[c(H+)-c(OH��)]��3c(C2O42��)-c(H2C2O4)+ c(HC2O4��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ��ɳ�и߶���ѧ�ڵ�һ��ģ���⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����16.8g��Fe��Fe2O3��Al��Al2O3��ɵĻ���������ȫ�ܽ���600mL2mol/L��������Һ�У��ռ�����״���µ�����8.96L����֪�������Fe��Fe2O3��Al��Al2O3�����������ֱ�Ϊ16.7%��16.1%��38.1%��29.1%����ʹ��Һ�еĽ���������ȫ����������Ӧ����3mol/LNaOH��Һ������� �� ����
A. 800mL B. 300mL C. 600mL D. 900mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡЭ���������ѧ�ڵ�һ���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڼ������ᣨC8H8O2��������ũҩ��ҽҩ���л�����ԭ�ϵĺϳɣ�Ҳ��Ŀǰ���ݼ������ݵ���Ҫԭ�ϣ����ڼ��������������������ͬ���칹�壺
����������������Һ��Ӧ ���������Ʊ���������Һ����������Ӧ
����������Ʒ�Ӧ�Ҿ��м��ķ����廯������ж����֣� ��
A. 10 B. 11 C. 12 D. 13
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com