
| A、把石灰石固体研细后与盐酸反应 |
| B、用MnO2作H2O2分解反应的催化剂 |
| C、把盛有Cu和稀硝酸的试管稍加热 |
| D、用10%H2SO4溶液代替30%H2SO4溶液与锌粒反应 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油分馏得到汽油、煤油和柴油 |
| B、石油裂解得到乙烯、丙烯、丁二烯 |
| C、天然气完全燃烧生成二氧化碳和水 |
| D、煤干馏生成焦炭、煤焦油、焦炉气和粗氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2 |
| B、生活污水 |
| C、SO2、NO2、可吸入颗粒 |
| D、废旧电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对废旧电池进行回收处理 |
| B、使用沼气、太阳能、风能等能源替代传统的煤炭 |
| C、对聚乙烯等塑料进行深埋或倾倒入大海 |
| D、出台法规保护生物物种多样性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
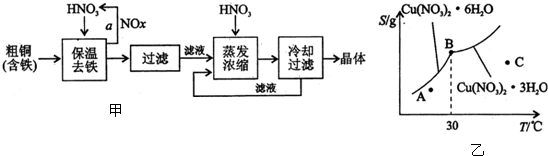
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| ||
| 一定条件 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com