
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 22.4L O2的物质的量约为1mol
B. 4.4g CO2含有的原子数为0.3NA
C. 1mol/L的CuSO4溶液中SO42—的物质的量为1mol
D. 标准状况下,11.2L H2O的物质的量约为1mol
科目:高中化学 来源: 题型:
【题目】某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。回答下列问题:
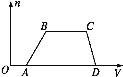
(1)溶液中一定含有的溶质是______________________(填化学式)。
(2)溶液中一定不含有的溶质是________________(填化学式)。
(3)溶液中可能含有的溶质是____(填名称),判断该物质是否存在的实验方法是____,若存在则现象是_______________________________________________。
(4)分别写出AB段、BC段发生反应的离子方程式:
①AB段为_______________________________________________________________;
②BC段为_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气脱硝脱碳主要原理为2NO(g)+2CO(g)![]() N2(g)+2CO2(g) +Q(Q>0)。一定条件下密闭容器
N2(g)+2CO2(g) +Q(Q>0)。一定条件下密闭容器
中,用传感器测得该反应在不同时间 NO 和 CO 浓度如下表:
时间/s | 0 | 1 | 2 | 3 | 4 |
c(NO)/molL-1 | 9.50×10-3 | 4.50×10-3 | 2.50×10-3 | 1.50×10-3 | 1.50×10-3 |
c(CO)/molL-1 | 9.00×10-3 | 4.00×10-3 | 2.00×10-3 | 1.00×10-3 | 1.00×10-3 |
完成下列填空:
(1) 写出该反应的平衡常数表达式:_________。 温度升高,二氧化碳气体的浓度将______(填“变大”、“变小”或“不变”)。
(2)前 2s 内的氮气的平均反应速率是:v(N2)=______mol/(Ls);达到平衡时,CO 的转化率为:_____。
(3)工业上常采用“ 低温臭氧氧化脱硫脱硝” 技术来同时吸收 SO2 和氮的氧化物气体(NOx ),以获得(NH4)2SO4 的稀溶液。在此溶液中,水的电离程度是受到了_____(填“促进”、“抑制”或“没有影响”);
若往(NH4)2SO4溶液中再加入少量稀盐酸,则![]() 值将_____(填“变大”、“变小”或“不变”)。
值将_____(填“变大”、“变小”或“不变”)。
(4)如果向 BaCl2 溶液中通入足量 SO2 气体,没有沉淀生成,继续滴加一定量的氨水后,则会生成白色沉淀。用平衡移动原理解释上述现象:___________________________。
(5)向另一种可溶性钡盐溶液中通入少量 SO2 气体,会立即看到白色沉淀。该沉淀的化学式为_____; 原可溶性钡盐可能是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①⑩种元素,填写下列空白:
周期 | IA | IIA | ⅢA | IVA | VA | VIA | ⅦA |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)上述元素中,形成化合物种类最多的是______(填元素符号)。
(2)元素①、④和⑤形成的化合物的电子式是______,该化合物中存在的化学键类型是______。
(3)②、③、⑦三种元素原子半径由大到小的顺序是______(用元素符号表示)。
⑤、⑥、⑦、⑧、⑨、⑩六种元素形成的简单离子,半径最小的是_________,最大的是___________(填离子符号)。
(4)⑤、⑥、⑦三种元素最髙价氧化物对应水化物的碱性由强到弱的顺序是______(用对应物质的化学式表示)。
(5)最易形成离子键的两种元素代号是_____________。
(6)能比较元素⑨和⑩非金属性强弱的实验事实是______(填字母序号)。
a.⑨的氢化物的酸性比⑩的氢化物的酸性弱
b.⑩的单质R2与H2化合比⑨的单质Q与H2化合容易,且HR的稳定性比H2Q强
c.在⑨的氢化物H2Q的水溶液中通少量⑩的单质R2气体可置换出单质Q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( )
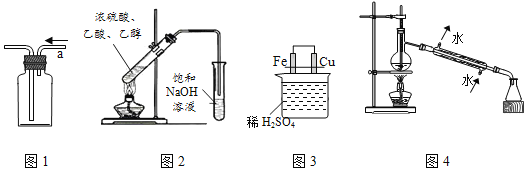
A. 用图1从a口进气可收集乙烯 B. 用图2制取并收集乙酸乙酯
C. 用图3比较Fe、Cu的金属活动性 D. 用图4进行石油的蒸馏实验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国利用合成气直接制烯烃获重大突破,其原理是
反应①:C(s)+1/2O2(g) = CO(g) ΔH1
反应②:C(s)+H2O(g) = CO(g)+H2(g) ΔH2
反应③:CO(g)+2H2(g) = CH3OH(g) ΔH3=-90.1 kJ·mol-1
反应④:2CH3OH(g) = CH3OCH3(g)+H2O(g) ΔH4,能量变化如图所示
反应⑤:3CH3OH(g)= CH3CH=CH2(g)+3H2O(g) ΔH5=-31.0 kJ·mol-1
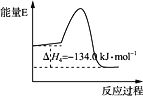
下列说法正确的是
A. 反应③使用催化剂,ΔH3减小
B. 反应④中正反应的活化能大于逆反应的活化能
C. ΔH1-ΔH2<0
D. 反应①和反应②,制取等量的CO,无论哪种途径,消耗的能量均相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC将合成化学元素第115号(Mc)提名为化学新元素,Mc的原子核最外层电子数是5,下列说法不正确的( )
A. Mc的原子核外有115个电子
B. Mc与N元素属于同一主族
C. Mc在同主族元素中金属性最强
D. 中子数为173的Mc核素符号是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物在水中的电离方程式不正确的是( )
A.CaCl2═Ca2++2Cl﹣B.NH4Cl═NH4++Cl﹣
C.KClO3═K++Cl﹣+3O2﹣D.HNO3═H++NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色环保水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,应用广泛。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应氧化产物是_____(填化学式)。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO、OH、FeO42-、Cl、H2O。
①写出并配平碱性条件下湿法制高铁酸钾的离子反应方程式:________________________________。
②每生成1molFeO42-转移________mol电子;若反应过程中转移了0.3mol电子,则还原产物的物质的量为________mol。
Ⅱ.氧化还原反应在生产生活中应用广泛,思考回答以下问题
已知:2Fe3++2I===2Fe2++I2,2Fe2++Br2===2Fe3++2Br,2Fe2++Cl2===2Fe3++2Cl
(1)含有1mol FeI2和2mol FeBr2的溶液中通入2mol Cl2,此时被氧化的离子是________。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c molCl2,当Br被氧化一半时,c为_______________(用含a、b的代数式表示)。
(3)已知:S2O![]() 具有较强的还原性,实验室可用I-测定测定K2S2O8样品的纯度:有关反应方程式为: I2+2S2O32-→2I+S4O62-,S2O82-+2I→2SO42-+I2,则S2O82-、S4O62-、I2氧化性强弱顺序为:____________。
具有较强的还原性,实验室可用I-测定测定K2S2O8样品的纯度:有关反应方程式为: I2+2S2O32-→2I+S4O62-,S2O82-+2I→2SO42-+I2,则S2O82-、S4O62-、I2氧化性强弱顺序为:____________。
(4)已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-;向含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如下图所示。
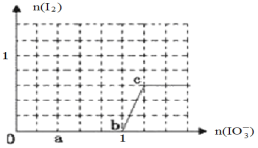
写出a点处还原产物是_______________;b点到c点反应的离子方程式________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com