

·ÖĪö ÓÉŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆæÉÖŖ£¬¢ŁĪŖH£¬¢ŚĪŖBe£¬¢ŪĪŖC£¬¢ÜĪŖMg£¬¢ŻĪŖAl£¬¢ŽĪŖP£¬¢ßĪŖCl£¬¢ąĪŖCa£¬¢įĪŖTi£¬¢āĪŖCu£¬
£Ø1£©dĒųŌŖĖŲŌŚø±×åŌŖĖŲŗĶ¹ż¶ÉŌŖĖŲĒų£»
£Ø2£©ŌŖĖŲ¢ŁµÄ6øöŌ×ÓÓėŌŖĖŲ¢ŪµÄ6øöŌ×ÓŠĪ³ÉµÄijÖÖ»·×“·Ö×ÓĪŖ±½£¬¢ŪŗĶ¢ßŠĪ³ÉµÄ³£¼ū»ÆŗĻĪļĪŖCCl4£»
£Ø3£©ŌŖĖŲµÄĢŲÕ÷µē×ÓÅŲ¼Ź½ĪŖnsnnpn+1£¬nÖ»ÄÜĪŖ2£¬ŌņøĆŌŖĖŲĪŖN£¬ŠĪ³ÉµÄ·Ö×ÓXĪŖNH3£»
£Ø4£©½šŹōŠŌŌ½Ē棬µŚŅ»µēĄėÄÜŌ½Š”£¬µ«MgµÄ3sČ«Āś£»·Ē½šŹōŠŌŌ½Ē棬µēøŗŠŌŌ½“ó£»
£Ø5£©ŌŖĖŲ¢ŚµÄĒāŃõ»ÆĪļÓėNaOHČÜŅŗ·“Ó¦·“Ӧɜ³ÉNa2BeO2£®
½ā“š ½ā£ŗÓÉŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆæÉÖŖ£¬¢ŁĪŖH£¬¢ŚĪŖBe£¬¢ŪĪŖC£¬¢ÜĪŖMg£¬¢ŻĪŖAl£¬¢ŽĪŖP£¬¢ßĪŖCl£¬¢ąĪŖCa£¬¢įĪŖTi£¬¢āĪŖCu£¬
£Ø1£©dĒųŌŖĖŲŌŚø±×åŌŖĖŲŗĶ¹ż¶ÉŌŖĖŲĒų£¬CuĪ»ÓŚdsĒų£¬Ö»ÓŠTiĪ»ÓŚdĒų£¬¹Ź“š°øĪŖ£ŗīŃ£»
£Ø2£©ŌŖĖŲ¢ŁµÄ6øöŌ×ÓÓėŌŖĖŲ¢ŪµÄ6øöŌ×ÓŠĪ³ÉµÄijÖÖ»·×“·Ö×ÓĪŖ±½£¬Į¢Ģå¹¹ŠĶĪŖĘ½Ćę£ØÕż£©Įł±ßŠĪ£¬¢ŪŗĶ¢ßŠĪ³ÉµÄ³£¼ū»ÆŗĻĪļĪŖCCl4£¬Óė¼×Ķé½į¹¹ĻąĖĘ£¬¾łĪŖÕżĖÄĆęĢ壬¹Ź“š°øĪŖ£ŗĘ½Ćę£ØÕż£©Įł±ßŠĪ£»ÕżĖÄĆęĢ壻
£Ø3£©ŌŖĖŲµÄĢŲÕ÷µē×ÓÅŲ¼Ź½ĪŖnsnnpn+1£¬nÖ»ÄÜĪŖ2£¬ŌņøĆŌŖĖŲĪŖN£¬×īĶā²ćÓŠ5øöµē×Ó£¬¹Ā¶Ōµē×ÓŹżĪŖ1£¬ŠĪ³ÉµÄ·Ö×ÓXĪŖNH3£¬æռ乹³ÉĪŖČż½Ē׶ŠĪ£¬ĪŖ¼«ŠŌ·Ö×Ó£¬
¹Ź“š°øĪŖ£ŗ¼«ŠŌ£»
£Ø4£©½šŹōŠŌMg£¾Al£¬µ«MgµÄ3sµē×ÓĪŖČ«Āś£¬ĪŖĪČ¶Ø½į¹¹£¬ŌņŌŖĖŲ¢ÜµÄµŚŅ»µēĄėÄÜ£¾ŌŖĖŲ¢ŻµÄµŚŅ»µēĄėÄÜ£»·Ē½šŹōŠŌŌ½Ē棬µēøŗŠŌŌ½“ó£¬ŌŖĖŲ¢ŽµÄµēøŗŠŌ£¼ŌŖĖŲ¢ßµÄµēøŗŠŌ£¬
¹Ź“š°øĪŖ£ŗ£¾£»£¼£»
£Ø5£©ŌŖĖŲ¢ŚµÄĒāŃõ»ÆĪļÓėNaOHČÜŅŗ·“Ó¦·“Ӧɜ³ÉNa2BeO2£¬øĆ·“Ó¦ĪŖBe£ØOH£©2+2NaOHØTNa2BeO2+2H2O£¬Ąė×Ó·“Ó¦ĪŖBe£ØOH£©2+2OH-ØTBeO22-+2H2O£¬
¹Ź“š°øĪŖ£ŗBe£ØOH£©2+2OH-ØTBeO22-+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĪ»ÖĆ”¢½į¹¹”¢ŠŌÖŹµÄÓ¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬Éę¼°ŌŖĖŲÖÜĘŚ±ķÖŠŌŖĖŲµÄ·ÖĒų”¢ŌŖĖŲÖÜĘŚ±ķÖŠŌŖĖŲµÄĪ»ÖĆ”¢¾§ĢåĄąŠĶ”¢·Ö×Ó¹¹ŠĶ”¢»Æѧ·“Ó¦µČ£¬×ŪŗĻŠŌ½ĻĒ棬ĢāÄæÄŃ¶Č½Ļ“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
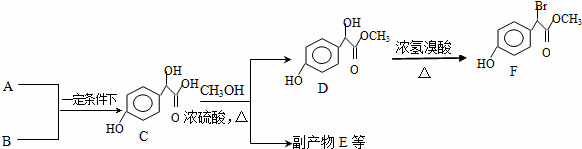
 £®
£®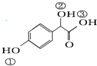 £©ÖŠ¢Ł”¢¢Ś”¢¢Ū£Ø“Ó×óµ½ÓŅ±ąŗÅ£©3øö-OHµÄĖįŠŌÓÉČõµ½ĒæµÄĖ³ŠņŹĒ£ŗ¢Ū£¾¢Ł£¾¢Ś£®
£©ÖŠ¢Ł”¢¢Ś”¢¢Ū£Ø“Ó×óµ½ÓŅ±ąŗÅ£©3øö-OHµÄĖįŠŌÓÉČõµ½ĒæµÄĖ³ŠņŹĒ£ŗ¢Ū£¾¢Ł£¾¢Ś£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
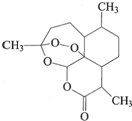 ÖŠ¹śŅ©Ń§¼ŅĶĄßĻßĻ»ńµĆ2015ÄźÅµ±“¶ūÉśĄķŅ½Ń§½±£®Ėż·¢ĻÖĮĖĒąŻļĖŲ--Ņ»ÖÖÓĆÓŚÖĪĮĘű¼²µÄŅ©Īļ£¬Ķģ¾ČĮĖČ«ĒņŹż°ŁĶņČĖµÄÉśĆü£®ĒąŻļĖŲµÄ½į¹¹ČēĶ¼ĖłŹ¾£®ĻĀĮŠÓŠ¹ŲĒąŻļĖŲµÄĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
ÖŠ¹śŅ©Ń§¼ŅĶĄßĻßĻ»ńµĆ2015ÄźÅµ±“¶ūÉśĄķŅ½Ń§½±£®Ėż·¢ĻÖĮĖĒąŻļĖŲ--Ņ»ÖÖÓĆÓŚÖĪĮĘű¼²µÄŅ©Īļ£¬Ķģ¾ČĮĖČ«ĒņŹż°ŁĶņČĖµÄÉśĆü£®ĒąŻļĖŲµÄ½į¹¹ČēĶ¼ĖłŹ¾£®ĻĀĮŠÓŠ¹ŲĒąŻļĖŲµÄĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ·Ö×ÓŹ½ĪŖC15H22O5 | |
| B£® | Ņ×ČÜÓŚŅŅĆѵČÓŠ»śČܼĮ | |
| C£® | æÉ·¢ÉśČ”“ś·“Ó¦£¬²»ÄÜ·¢ÉśŃõ»Æ·“Ó¦ | |
| D£® | ŌŚĒæĖį»ņĒæ¼īŠŌČÜŅŗÖŠ²»ÄÜĪČ¶Ø“ęŌŚ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōCuµÄ¾§ĢåµÄÅäĪ»ŹżĪŖ12 | |
| B£® | ½šŹō¼üŹĒ½šŹōŃōĄė×ÓÓė×ŌÓɵē×Ó¼äµÄĻą»„×÷ÓĆ | |
| C£® | ½šŹōµÄŃÓÕ¹ŠŌæÉŅŌÓƵē×ÓĘųĄķĀŪ½āŹĶ | |
| D£® | ½šŹōMg”¢Zn”¢Ti¶¼ŹĒĮł·½×īĆܶѻż£¬æÕ¼äĄūÓĆĀŹŹĒ68% |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ķ¬ĻµĪļ£ŗŅŅĖį”¢ČķÖ¬Ėį”¢Ó²Ö¬Ėį | B£® | Ķ¬Ī»ĖŲ£ŗė”¢ė®”¢ė° | ||
| C£® | Ķ¬ĖŲŅģŠĪĢå£ŗ½šøÕŹÆ”¢ŹÆÄ«”¢×ćĒņĻ© | D£® | Ķ¬·ÖŅģ¹¹Ģå£ŗÕįĢĒ”¢ĀóŃæĢĒ”¢ĘĻĢŃĢĒ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½ŚČÕŃ껚ŹĒijŠ©½šŹōŌŖĖŲŃęÉ«·“Ó¦Ėł³ŹĻÖ³öĄ“µÄÉ«²Ź | |
| B£® | Éś»īÖŠ³£ÓƵÄĖÜĮĻÖĘĘ·¼°Ļš½ŗÖĘĘ·¶¼ĪŖøß·Ö×Ó²ÄĮĻ | |
| C£® | ĻņÅ£ÄĢÖŠ¼ÓČė¹ūÖ»į²śÉś³Įµķ£¬ÕāŹĒŅņĪŖĖį¼ī·¢ÉśĮĖÖŠŗĶ·“Ó¦ | |
| D£® | æÉÓĆÕŗÅØŃĪĖįµÄĆŽ°ō¼ģŃéŹäĖĶ°±ĘųµÄ¹ÜµĄŹĒ·ńĀ©Ęų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā


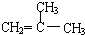 £®
£®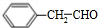 £»F·Ö×ÓÖŠ×ī¶ąÓŠ15øöŌ×Ó¹²Ćę£®
£»F·Ö×ÓÖŠ×ī¶ąÓŠ15øöŌ×Ó¹²Ćę£®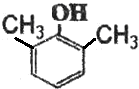 £Ø»ņ
£Ø»ņ ”¢
”¢ £©£®
£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
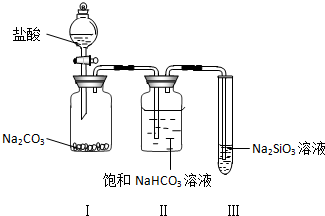
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com