
【题目】已知A、B、C、D四种短周期元素的核电荷数依次增大.A原子s轨道电子数是p轨道电子数的两倍,C原子的L能层中有两对成对电子,C、D同主族. E、F是第四周期元素,且E位于周期表中ds区,F原子核外有33种不同运动状态的电子.根据以上信息用相应的元素符号填空:
(1)E+核外电子排布式为 , FC43﹣离子的空间构型为 , 与其互为等电子体的一种有机分子为(填化学式).
(2)B元素所在周期第一电离能最大的元素是(填元素符号).
(3)D所在周期元素最高价氧化物对应的水化物中,酸性最强的是(填化学式);能导电的A单质与B、D、E的单质形成的晶体相比较,熔点由高到低的排列顺序是(填化学式).
(4)已知EDC4溶液中滴入氨基乙酸钠(H2N﹣CH2﹣COONa)即可得到配合物A.其结构如图所示: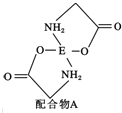
①配合物A中碳原子的轨道杂化类型为 .
②1mol氨基乙酸钠(H2N﹣CH2﹣COONa)含有σ键的数目为 .
(5)化合物F2C3常用于标定未知浓度的酸性KMnO4溶液,反应生成F的最高价含氧酸,该反应的离子方程式是 .
【答案】
(1)1s22s22p63s23p63d10;正四面体;CCl4
(2)Ne
(3)HClO4;C>Cu>S>N2
(4)sp3、sp2;8×6.02×1023
(5)5As2O3+4MnO ![]() +9H2O+12H+═10H3AsO4+4Mn2+
+9H2O+12H+═10H3AsO4+4Mn2+
【解析】解:A、B、C、D四种短周期元素的核电荷数依次增大,A原子s轨道电子数是p轨道电子数的两倍,原子核外电子排布为1s22s22p2 , 则A为碳元素;C原子的L能层中有两对成对电子,原子核外电子排布式为1s22s22p4 , 则C为O元素;B的原子序数介于碳、氧之间,则B为N元素;C、D同主族,则D为S元素; E、F是第四周期元素,且E位于周期表中ds区,结合(1)可以形成E+ , 则E为Cu;F原子核外有33种不同运动状态的电子,则F为As.(1)Cu+核外电子排布式为1s22s22p63s23p63d10 , AsO43﹣离子中As原子孤电子对数= ![]() =0,价层电子对数4+0=4,故为正四面体构型,与其互为等电子体的一种有机分子为CCl4 , 所以答案是:1s22s22p63s23p63d10;正四面体;CCl4;(2)N元素所在周期第一电离能最大的元素是Ne,所以答案是:Ne;(3)S所在周期元素最高价氧化物对应的水化物中,酸性最强的是HClO4;能导电的A单质为石墨,属于混合晶体,沸点很高,氮气常温下为气体,硫为分子晶体,沸点比较低,Cu为金属晶体,沸点比硫单质高,熔点由高到低的排列顺序是C>Cu>S>N2 , 所以答案是:HClO4;C>Cu>S>N2;(4)①亚甲基中C原子形成4个σ键、C=O中C原子形成3个σ键,均没有孤对电子,碳原子的轨道杂化类型为sp3、sp2 , 所以答案是:sp3、sp2 ;②1mol氨基乙酸钠(H2N﹣CH2﹣COONa)含有8molσ键,即含有8×6.02×1023个σ键,
=0,价层电子对数4+0=4,故为正四面体构型,与其互为等电子体的一种有机分子为CCl4 , 所以答案是:1s22s22p63s23p63d10;正四面体;CCl4;(2)N元素所在周期第一电离能最大的元素是Ne,所以答案是:Ne;(3)S所在周期元素最高价氧化物对应的水化物中,酸性最强的是HClO4;能导电的A单质为石墨,属于混合晶体,沸点很高,氮气常温下为气体,硫为分子晶体,沸点比较低,Cu为金属晶体,沸点比硫单质高,熔点由高到低的排列顺序是C>Cu>S>N2 , 所以答案是:HClO4;C>Cu>S>N2;(4)①亚甲基中C原子形成4个σ键、C=O中C原子形成3个σ键,均没有孤对电子,碳原子的轨道杂化类型为sp3、sp2 , 所以答案是:sp3、sp2 ;②1mol氨基乙酸钠(H2N﹣CH2﹣COONa)含有8molσ键,即含有8×6.02×1023个σ键,
所以答案是:8×6.02×1023;(5)化合物As2O3常用于标定未知浓度的酸性KMnO4溶液,反应生成H3AsO4 , 该反应的离子方程式是:5As2O3+4MnO4﹣+9H2O+12H+═10H3AsO4+4Mn2+ ,
所以答案是:5As2O3+4MnO4﹣+9H2O+12H+═10H3AsO4+4Mn2+ .


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 用加热分解的方法区分碳酸钠和碳酸氢钠两种固体
B. 由矿盐(主要成分是NaCl,还含有SO![]() 等其他可溶性杂质的离子)生产食盐,除去SO
等其他可溶性杂质的离子)生产食盐,除去SO![]() 最合适的试剂是BaCl2
最合适的试剂是BaCl2
C. 用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液
D. 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数,下列说法中正确的是( )
A. 1 mol水含有的氢原子数目为NAB. 1 mol氩气分子所含的原子数目为2NA
C. 0.5 mol碳酸钠中含有的钠离子为0.5NAD. 0.5 mol硝酸中含有的氧原子为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是 ( )
A. ②①④⑤③ B. ②⑤④①③ C. ④①②⑤③ D. ①②④⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1molL﹣1氢氧化钠溶液与0.06molL﹣1硫酸溶液等体积混合,该混合溶液的pH等于( )lg2=0.3.
A.1.7
B.2.0
C.12.0
D.11.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的分子式为C10H14 , 它不能使溴水褪色,但可使KMnO4酸性溶液褪色,分子结构中只含有一个烷基,符合条件的烃有( )
A.2种
B.3种
C.4种
D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空
(1)2SO2(g)+O2(g) △ v 2 O 5 2SO3(g);△H=﹣196.6KJ/mol,是制备硫酸的重要反应.下列关于该反应的叙述正确的是 . (填字母)
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1 , c2 , 则时间间隔t1~t2内,SO3(g)生成的平均速率为u= c 2 c 1 t 2 t 1
E.使用催化剂V2O5能提高SO2的转化率
F.使用催化剂V2O5会改变该反应的△H
(2)判断该反应达到平衡状态的标志是 .(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.在体积不变的容器中,气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.在体积不变的容器中混合气体,的密度保持不变
f.SO2、O2、SO3的浓度比保持不变.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向500mL稀硝酸中加入一定质量的铁粉,铁粉完全溶解后,放出NO气体5.6L(标准状况),同时溶液质量增加9.3g,下列判断正确的是( )
A.原溶液中投入铁粉物质的量是0.25mol
B.原溶液中的HNO3浓度是2.0mol/L
C.反应后的溶液中还可以溶解9.6g铜
D.反应后的溶液中c(Fe2+):c(Fe3+)=1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com