

 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
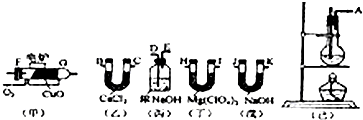
查看答案和解析>>
科目:高中化学 来源:知识精讲与能力训练 高三化学 题型:022
测定有机物中碳和氢的质量分数最常用的方法是燃烧分析法.某实验工作者将3.2g气体样品放在氧气流中充分燃烧,将燃烧后的产物依次通过无水CaCl2和碱石灰,结果无水CaCl2增重7.2g,碱石灰增重8.8g.
(1)该有机物中碳的质量分数是________,氢的质量分数是________.
(2)实验测知,在标准状况下,0.5g该气体占体积700mL,则这种烃的式量是________.
(3)该有机物的化学式是________,电子式是________,结构式是________.
查看答案和解析>>
科目:高中化学 来源: 题型:

回答下列问题:
(1)若产生的气体由左向右流向,各装置导管的连接顺序是:G接E、F接___________、___________接___________、___________接___________。
(2)装置Ⅱ的作用是___________;装置Ⅲ的作用是___________。
(3)装置Ⅳ中的化学方程式______________________;装置Ⅴ中的化学方程式______________________。
(4)实验前称得Ⅰ、Ⅱ两装置的质量分别为m1 g和n1 g,实验完毕,称得Ⅰ、Ⅱ两装置的质量分别变为m2 g和n2 g,则乙炔分子中碳原子和氢原子的原子个数比为___________(列出算式)。经多次实验发现测得的结果与理论值存在一定偏差,你认为原因可能为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)测定有机物中碳和氢的质量分数,常用燃烧分析法,用氧化铜为催化剂,在750℃左右使有机物在氧气流中全部氧化成CO2和H2O;分别用装有固体NaOH和Mg(ClO4)2的吸收管吸收CO2和H2O。某课外活动小组,设计利用下图所示装置制取纯净干燥的乙烯,并测定乙烯分子中碳、氢原子的个数比;甲为燃烧管,当乙烯和氧气通过时,由于催化剂的存在而不会发生爆炸,乙烯被氧化成CO2和H2O。请回答下列问题:
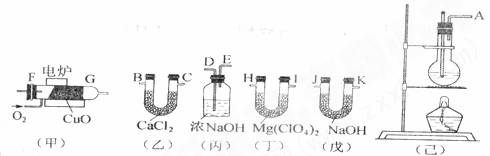
(1)整套装置的连接顺序(按气流方向从左到右填写仪器的接口字母):
(不考虑吸收空气的CO2或H2O)
A接▲ , _▲_接___▲___,_▲____接 ▲ , ▲ 接▲ , ▲ 接J…
(2)烧瓶中的试剂是浓硫酸和酒精,浓硫酸的作用是: ▲ ;
(3)实验时应使烧瓶中溶液的温度迅速升至170℃,原因是 ▲ ;
(4)乙装置的作用是 ▲ ,丙装置的作用是 ▲ ;
(5)若实验前后,丁增重ag、戊增重bg,则测得乙烯分子中C、H原子的个数比为
▲ ;
(6)若测得的比值偏高,导致这种误差的可能的原因是 ▲ ;
A.乙烯中混有少量的CO B.乙烯进入燃烧管时,含有少量的水蒸气
C.乙烯中混有少量的乙醚(C2H5OC2H5) D.乙烯进入燃烧管时,含有少量的CO2
(7)若仍用此装置测定某烃A的化学式。经测定:丁增重4.5g、戊增重8.8g,
则A的分子式为 ▲ ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com