
分析 (1)同质量的烃CxHy,$\frac{y}{x}$值越大,完全燃烧耗氧量越多,生成的H2O物质的量越大,CO2的物质的量越少.同状况、同体积、同物质的量的烃完全燃烧,耗氧量取决于x+$\frac{y}{4}$的相对大小;
(2)根据2-OH~H2,进行计算;1400C发生分子间取代反应,生成醚,同种分子和不同种分子之间来考虑.
解答 解:(1)同质量的烃CxHy,$\frac{y}{x}$值越大,完全燃烧耗氧量越多,生成的H2O物质的量越大,CO2的物质的量越少.同状况、同体积、同物质的量的烃完全燃烧,耗氧量取决于x+$\frac{y}{4}$的相对大小;
CH4、C2H4、C2H6、C3H6、C3H8五种有机物中,$\frac{y}{x}$值分别为4、2、3、2、$\frac{8}{3}$,故CH4全燃烧时耗O2的量最多,生成水最多的是CH4,
CH4、C2H4、C2H6、C3H6、C3H8五种有机物中,x+$\frac{y}{4}$的值分别为2、3、3.5、4.5、5,故同物质的量的以上物质完全燃烧时耗O2的量最多的是C3H8,
故答案为:CH4;C3H8;CH4;
(2)由2-OH~H2可知,分子中羟基的物质的量越多,放出氢气的量越多,所以相同物质的量时丙三醇放出氢气最多,乙醇、1-丙醇、2-丙醇,同种分子间得3种醚,不同种分子间得3种醚,共6种,故答案为:C;6.
点评 本题考查了有机物结构与性质,涉及了化学反应的简单计算,题目难度中等,注意掌握醇的结构与性质,(2)为难点和易错点,注意明确计算方法.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示的铜-锌原电池中,
如图所示的铜-锌原电池中,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,LiMn2O4发生氧化反应 | |
| B. | 放电时,正极反应为:Li++LiMn2O4+e-═Li2Mn2O4 | |
| C. | 充电时,LiMn2O4发生氧化反应 | |
| D. | 充电时,阳极反应为:Li++e-═Li |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 部分卤代烃可用作灭火剂 | |
| B. | 甲醛的水溶液(福尔马林)可用于防腐 | |
| C. | 酚类化合物有毒,不能用于杀菌消毒 | |
| D. | 乙二醇可用于配制汽车防冻液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
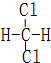 和
和 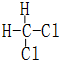 同一种物质.
同一种物质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是银白色的柔软金属,密度都比水小 | |
| B. | 单质在空气中燃烧生成的都是过氧化物 | |
| C. | 单质的熔沸点随着原子序数的增加而升高 | |
| D. | 碱金属单质与水剧烈反应生成碱和氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 暖冰中水分子是一种非常稳定的化合物,这是由于氢键所致 | |
| B. | 暖冰中水分子的各原子均满足8电子稳定结构 | |
| C. | 水凝固形成20℃时的“暖冰”所发生的变化是化学变化 | |
| D. | 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com