
| A、澄清的石灰水与盐酸反应 Ca(OH)2+2H+═Ca2++2H2 O |
| B、钠与水的反应 Na+2H2 O═Na++2OH-+H2↑ |
| C、铜片插入硝酸银溶液 Cu+Ag+═Cu2++Ag |
| D、大理石溶于醋酸 CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2加入水制备O2:2O22-+2H2O=4OH-+O2↑ |
| B、用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O |
| C、向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| D、向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
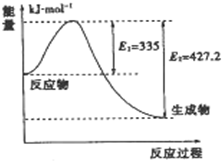 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com