
分析 (1)氯气与水反应生成盐酸和次氯酸,反应的化学方程式为:Cl2+H2O?HCl+HClO,氯气的化合价既升高又降低,所以氯气既是氧化剂也是还原剂,氧化产物是次氯酸,由此分析解答;
(2)用液氯作为自来水的杀菌剂,起作用的是HClO,所以液氯加入水中后含氯的物质有氯单质、HClO和HCl;NH2Cl中氮氯键,共用电子偏向氮,偏离氯,所以氮是负3价,而氯是+1价,与水反应根据相反相成,水中电离的氢离子与氮结合,氢氧化根与氯结合生成次氯酸,由此分析解答.
解答 解:(1)氯气与水反应生成盐酸和次氯酸,反应的化学方程式为:Cl2+H2O?HCl+HClO,氯气的化合价既升高又降低,所以氯气既是氧化剂也是还原剂,氧化产物是次氯酸,
故答案为:Cl2+H2O?HCl+HClO;Cl2;HClO;氧化剂和还原剂是同一种物质中的同一种元素;这种元素化合价既升高又降低;
(2)用液氯作为自来水的杀菌剂,起作用的是HClO,所以液氯加入水中后含氯的物质有氯单质、HClO和HCl;NH2Cl中氮氯键,共用电子偏向氮,偏离氯,所以氮是负3价,而氯是+1价,与水反应根据相反相成,水中电离的氢离子与氮结合,氢氧化根与氯结合生成次氯酸,反应H2O+NH2Cl═NH3↑+HClO中无化合价的变化,是复分解反应,故选BD,故答案为:HCl;BD.
点评 本题以氯元素及其化合物之间的转化为载体考查氧化还原反应,明确元素化合价与物质性质关系是解本题关键,注意:同一种元素之间发生氧化还原反应,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 醋酸钡与硫酸反应:Ba2++SO42-→BaSO4↓ | |
| B. | 金属铝溶于稀硫酸:Al+2H+→Al3++H2↓ | |
| C. | 将氯气溶于水制备次氯酸:Cl2+H2O→2H++Cl-+ClO- | |
| D. | 碳酸氢钠和盐酸反应:HCO3-+H+→CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
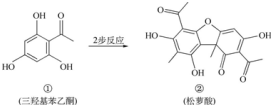
| A. | 有机物①的分子式为C8H6O4 | |
| B. | 有机物①在一定条件下能发生取代、加成和氧化反应 | |
| C. | 可用FeCl3溶液检验②中是否含有杂质① | |
| D. | 相同物质的量①、②与足量NaOH溶液反应,消耗NaOH的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl3 NaOH KCl | B. | KCl Na2CO3 Na2SO4 | ||
| C. | BaCl2 NaCl Na2SO4 | D. | NaCl AgNO3 KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
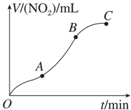
| A. | OA段表示开始时,反应速率稍慢 | |
| B. | AB段表示反应速率较快,一定因为产物有催化作用 | |
| C. | BC段表示随时间增加,反应速率逐渐增大 | |
| D. | BC段表示反应速率最快,在该时间段内收集到的气体最多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=b | B. | a=2b | C. | 2a=b | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加铁的量 | B. | 加热 | ||
| C. | 滴加少量CuSO4溶液 | D. | 不用铁片,改用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com