
| m |
| M |
| m |
| M |
| 23g |
| 23g/mol |


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中Ca2+数目减少 |
| B、溶液中c(Ca2+)增大 |
| C、溶液中c(Ca2+)减小 |
| D、溶液pH值增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子序数一定是Z>X>Y |
| B、X、Z两种元素的金属性X>Z |
| C、Z的最高价氧化物一定能溶于X、Y的最高价氧化物的水化物 |
| D、工业上获得X、Z单质的方法主要是电解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O、D2O、T2O互为同位素 |
| B、pH=1的溶液中,K+、Na+、NO3-、S2O32-不能大量共存 |
| C、元素周期表中从上至下同主族元素的氢化物的熔、沸点依次升高 |
| D、乙炔、氢气、铁分别与氯气反应,都会因用量或条件不同而生成不同产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| B、标准状况下,22.4L己烷中共价键数目为19NA |
| C、由SO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| D、1L浓度为1mol?L-1的Na2CO3溶液中含有NA个CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
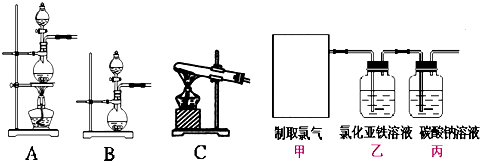
查看答案和解析>>
科目:高中化学 来源: 题型:
| 有机物 | 乙烯 | 乙炔 | 环已烷 | 苯 |
| Ω | 1 | 2 | 1 | 4 |
| A、1molΩ=3的不饱和链烃再结合6molH2即达到饱和 |
| B、C10H8的Ω=7 |
| C、C4H8的不饱和度与C3H6、C2H4的不饱和度不相同 |
| D、CH3CH2CH=CH2与环丁烷的不饱和度相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com