
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:2015-2016学年陕西西安高新一中高一下期末化学试卷(解析版) 题型:填空题
I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步:
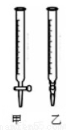
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号) 。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______中。(从图中选填“甲”或“乙”)
(3)下列操作会引起实验结果偏大的是:______(填编号)
A.在锥形瓶装液前,留有少量蒸馏水
B.滴定前,滴定管尖嘴有气泡,滴定后无气泡
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视 。判断到达滴定终点的现象是:锥形瓶中溶液 。
(5)以下是实验数据记录表
滴定次数 | 盐酸体积mL | NaOH溶液体积读数(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.00 | 21.30 |
2 | 20.00 | 0.00 | 16.30 |
3 | 20.00 | 0.00 | 16.32 |
通过计算可得,该盐酸浓度为:______ mol•L-1(计算结果保留4位小数)
II、利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤1:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤2:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤:1相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
则BaCl2溶液浓度为______________________ mol·L-1。若步骤2中滴加盐酸时有少量待测液溅出,则Ba2+浓度的测量值将___________(填“偏大”或“偏小”)。
【答案】I、(1)①④;(2)乙;(3)B;
(4)锥形瓶内颜色;由无色变成浅红色,且半分钟内不变色。(5)0.1631;
II、(V0b-V1b)/y ;偏大。
【解析】
试题分析:(1)①根据碱式滴定管在装液前应用所装液体进行润洗,用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上,碱式滴定管未用标准氢氧化钠溶液润洗就直接注入标准NaOH溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=V(标准)×c(标准) ÷V(待测),可知c(标准)偏大;④酸碱指示剂酚酞是弱电解质,也会反应消耗酸或碱,为了减少实验误差,酚酞一般滴加1滴或2滴,错误;其余操作正确;(2)NaOH是碱,容易与玻璃中的SiO2发生反应,所以应该装在碱式滴定管乙中;(3)A.在锥形瓶装液前,留有少量蒸馏水,由于不影响酸、碱的物质的量,所以对滴定操作无影响,错误;B.滴定前,滴定管尖嘴有气泡,滴定后无气泡,使标准溶液体积偏大,导致待测溶液的浓度偏高,正确;C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗,操作正确,不会产生误差,错误;D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失,则待测溶液体积偏少,反应消耗标准酸溶液的体积偏小,使测得浓度偏低,错误。(4)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视锥形瓶内颜色;判断到达滴定终点的现象是:锥形瓶中溶液由无色变成浅红色,且半分钟内不变色。(5)酸碱发生中和反应时二者的物质的量相等。根据实验数据可知,第一次实验数据误差太大,舍弃,V(NaOH)= (16.30+16.32)÷2=16.31mL,c(NaOH)·V(NaOH)=c(HCl)·V(HCl),所以c(HCl)=[ c(NaOH)·V(NaOH)]÷V(HCl)= [0.2000 mol·L-1×16.31mL]÷20.00mL=0.1631mol/L;II、根据方程式可知氢离子的物质的量与溶液中Ba2+的物质的量相等。步骤Ⅱ:待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL,则发生2CrO42-+2H+=Cr2O72-+H2O的盐酸的物质的量为:V1×10-3×bmol,步骤Ⅰ:用b mol•L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL,加入的总盐酸的物质的量:V0×10-3×bmol,Ba2++CrO42-=BaCrO4↓,与Ba2+反应的CrO42-的物质的量为V0×10-3×bmol-V1×10-3×bmol=(V0 -V1)b×10-3mol,步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,所以BaCl2溶液的浓度为:(V0 -V1)b×10-3mol ÷y×10?3mol/L=(V0b-V1b)/ymol/L;若步骤Ⅱ中滴加盐酸时有少量待测液溅出,V1减小,则Ba2+浓度测量值将偏大。
考点:考查酸碱中和滴定的有关知识。
【题型】实验题
【适用】较难
【标题】【百强校】2015-2016学年陕西西安高新一中高一下期末化学试卷(带解析)
【关键字标签】
【结束】
氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)已知:2NO2(g)  N2O(g) △H1 2NO2(g)
N2O(g) △H1 2NO2(g)  N2O(l) △H2
N2O(l) △H2
下列能量变化示意图中,正确的是(选填字母) 。

(2)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如下图)
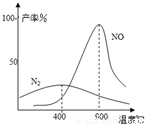
温度较低时以生成 为主,温度高于900℃时,NO产率下降的原因是 。
(3)火箭升空需要高能的燃料,经常是用四氧化二氮和联氨(N2H4)作为燃料,工业上利用氨气和氢气可以合成氨气,氨又可以进一步制备联氨等。
已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ•mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ•mol-1
NO2(g)  1/2 N2O4(g) △H=-26.35kJ•mol-1
1/2 N2O4(g) △H=-26.35kJ•mol-1
①写出气态联氨在气态四氧化二氮中燃烧生成氮气和水蒸气的热化学方程式: 。
②用氨和次氯酸钠按一定物质的量之比混合反应可生成联氨,该反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一下期末化学试卷(解析版) 题型:选择题
阿波罗宇宙飞船上使用的是氢——氧燃料电池,其电极总反应式为:2H2+O2═2H2O;电解质溶液为KOH溶液,反应保持在较高温度,使水蒸发,下列叙述正确的是
A.此电池能见到浅蓝色火焰
B.H2为正极,O2为负极
C.工作时电解液的OH-的物质的量不断增加
D.电极反应为:负极H2失电子;正极O2得电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南师大附中高一实验班下期末理综化学卷(解析版) 题型:填空题
在下列各组物质中(填选项号):
A.O2和O3
B.16O和18O
C.蔗糖和麦芽糖
D.CH4和CH3(CH2)2CH3
E.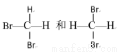
(1)互为同位素的是:_______;(2)互为同素异形体的是:_______;
(3)属于同系物的是:________;(4)互为同分异构体的是_________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南琼海嘉积中学高一下期末文科化学试卷(解析版) 题型:选择题
苯与乙烯相比较,下列叙述正确的是( )
A. 都容易发生取代反应
B. 都能在空气中燃烧
C. 苯不能发生加成反应
D. 苯能被KMnO4氧化
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南琼海嘉积中学高一下期末文科化学试卷(解析版) 题型:选择题
能源可分为一次能源和二次能源,下列叙述正确的是( )
A.天然气是二次能源 B.石油是二次能源
C.电能是一次能源 D.水力是一次能源
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一下期末化学试卷(解析版) 题型:选择题
已知COCl2(g)  CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施能提高COCl2转化率的是
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施能提高COCl2转化率的是
①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体
A.①②④ B.①④⑥ C.②③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期末化学试卷(解析版) 题型:选择题
下列有机物命名正确的是( )
A. 1, 3, 4-三甲苯
1, 3, 4-三甲苯
B. 2-甲基-2-氯丙烷
2-甲基-2-氯丙烷
C. 2-甲基-1-丙醇
2-甲基-1-丙醇
D. 2-甲基-3-丁炔
2-甲基-3-丁炔
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com