
| 时间t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCL3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
| ||
| 50s |
| 0.8mol |
| 2.0L |
| 0.2mol |
| 2.0L |
| c(PCl3)?c(Cl2) |
| c(PCl5) |
| 0.1×0.1 |
| 0.4 |
| a+0.1 |
| 2 |
| ||
| 0.2 |
| x |
| 3 |
| 4 | 4.2×10-16 |
| 4 | 4.2 |
| 1.8×10-10 |
| 1.8 |
| 4 | 4.2 |
| 60mol |
| 20mol |


 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源:不详 题型:单选题
 2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )
2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )| A.v(H2)="0.7" mol·(L·min)–1 | B.v(NH3)="0.3" mol·(L·min)-1 |
| C.v(H2)="0.2" mol·(L·min)-1 | D.v(H2)="0.15" mol·(L·min)-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.v(A2)=0.8mol?L-1?s-1 | B.v(A2)=30mol?L-1?min-1 |
| C.v(AB3)=1.0mol?L-1?s-1 | D.v(B2)=1.2mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.44s | B.1s | C.0.33s | D.2s |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.3mol?L-1s-1 | B.0.6mol?L-1s-1 |
| C.1.0mol?L-1s-1 | D.0.7mol?L-1s-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO2(g) + H2(g) △H < 0,下列措施能提高反应速率的有 (不定项选择)。
CO2(g) + H2(g) △H < 0,下列措施能提高反应速率的有 (不定项选择)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.加入铜粉,v(H2)增大 |
| B.加入NaHSO4固体,v(H2)不变 |
| C.加入水,锌不与水反应,v(H2)不变 |
| D.加入NaCl固体,会增大Cl-浓度,使v(H2)增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )A.该反应的化学平衡常数表达式是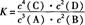 |
| B.此时,B的平衡转化率是35% |
| C.增大该体系的压强,平衡向右移动,化学平衡常数增大 |
| D.增大C,B的平衡转化率不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况下) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com