
| 2 |
| 3 |
| A��ZO3��ˮ��Ӧ�γɵĻ����������ӻ����� |
| B��ճ���Թ��ڱ��ϵ�Z������YZ2ϴ�� |
| C������������Ӧˮ����ļ��ԣ�X��W |
| D��Xλ�ڽ�����ǽ����ķֽ��ߴ������������뵼����� |
| 2 |
| 3 |
| 2 |
| 3 |


 ��������ϵ�д�
��������ϵ�д� ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Ͷ��黥Ϊͬϵ���ѧ�������� |
| B������Ͷ����������Ӧ��Ϊȡ����Ӧ |
| C��C3H8û��ͬ���칹�壬C4H10������ͬ���칹�� |
| D���������ı���Ͷ�����ȫȼ��ʱ�����ߺ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +2 | +6��-2 | -2 |
| A��L2+��R2-����������� |
| B����̬�⻯������ȶ��ԣ�H2T��H2R |
| C��M��T�γɵĻ����������ڰ�ˮ��Һ |
| D����ͬ�����£�������ͬŨ��ϡ���ᷴӦ�����ʣ�M��L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ�б������뱻��ԭ��Ԫ�أ���ԭ�ӵ����ʵ���֮��Ϊ1��2 |
| B��NF3��NH3��ѧ���ʵIJ�ͬ����F��H��Ԫ�طǽ����ԵIJ������� |
| C��NF3һ��й©������NaOH��Һ���ܣ�ֻ��NaF��NaNO3��H2O���� |
| D������Ӧ��ת��0.2mol���ӣ������ɵ�NO�������ԼΪ4.48L����״���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��pH=1����Һ�У�Fe2+��ClO-��Na+��SO42- |
| B���ں��϶�Al3+����Һ�У�K+��Cl-��HCO3- |
| C��һС����Ͷ�뵽CuSO4��Һ�У�2Na+Cu2+�TCu+2Na+ |
| D��ͭ����ϡ���3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
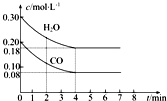 ��1����һ���Ϊ10L�������У�ͨ��һ������CO��H2O���� 800��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0��CO��H2O�����ʵ���Ũ�ȱ仯��ͼ��ʾ����
��1����һ���Ϊ10L�������У�ͨ��һ������CO��H2O���� 800��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0��CO��H2O�����ʵ���Ũ�ȱ仯��ͼ��ʾ����| C����I-��/mol?L-1 | C����Fe3+��/mol?L-1 | v/mol?L-1?s-1 | |
| �� | 0.20 | 0.80 | 0.032k |
| �� | 0.60 | 0.40 | 0.144k |
| �� | 0.80 | 0.20 | 0.128k |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��Ҫ���������С�⣮
��Ҫ���������С�⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com