
����Ŀ��ij�Ż��������Ҫ�ɷ���FexS(SΪ-2��)���Ⱥ���Fe2+�ֺ���Fe3+ ����һ�����ĸôŻ�������l00 mL������ǡ����ȫ��Ӧ��ע����ʯ�������ɷֲ������ᷴӦ��������2.4 g���ʡ�0. 425 mol FeCl2��һ����H2S���壬����Һ����Fe3+��������˵������ȷ����
A.����������ʵ���Ũ��Ϊ8.5 mol/L
B.���ɵ�H2S�����ڱ�״���µ����Ϊ9.52 L
C.�ôŻ�����FexS�У�x=0. 85
D.�ôŻ�����FexS�У�Fe2+�����ʵ���Ϊ0. 15mol
���𰸡�D
��������
n(S)=![]() =0.075mol������ת�Ƶ����غ��n(Fe3+)=
=0.075mol������ת�Ƶ����غ��n(Fe3+)=![]() =0.15mol����n(Fe2+)=0.425mol0.15mol=0.275mol������Fe2+��Fe3+�����ʵ���֮��=
=0.15mol����n(Fe2+)=0.425mol0.15mol=0.275mol������Fe2+��Fe3+�����ʵ���֮��=![]() =11:6��
=11:6��
A.����ǡ�÷�Ӧ����FeCl20.425mol��������ԭ���غ�ã�c(HCl)=![]() =8.5mol/L����A��ȷ��
=8.5mol/L����A��ȷ��
B.������ԭ�ӡ���ԭ���غ�ã�n(H2S)=1/2n(HCl)=n(FeCl2)=0.425mol����V(H2S)=0.425mol��22.4L/mol=9.52L����B��ȷ��
C.FexS��n(S)=0.075mol+0.425mol=0.5mol��n(Fe)=0.425mol������n(Fe)��n(S)=0.425mol��0.5mol=0.85������x=0.85����C��ȷ��
D.����������������Fe2+�����ʵ���Ϊ0.275mol����D����
��ѡD��


 ����С��ʿ���������ϵ�д�
����С��ʿ���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о��ⵥ������ط�Ӧ�е�ת�������ɾ�����Ҫ��ֵ��
(1)TaS2������һ��ǿ������ά���ϣ���һ�������¿ɷ������·�Ӧ��
TaS2(s)��2I2(g) ![]() TaI4(g)��S2(g) ��H��0
TaI4(g)��S2(g) ��H��0
��T��ʱ�������Ϊ2 L�����ܱ������м���0.3 mol I2(g)��0.3 mol TaS2(s)���ﵽƽ��ʱ��I2(g)�����ʵ���Ϊ0.1 mol���÷�Ӧ��ƽ�ⳣ��Ϊ__________����ƽ�����������ٳ���0.3 mol I2(g)������˵����ȷ����__________������ĸ����
A����2v(I2)����v(S2)��ʱ����Ӧ�����µ�ƽ��
B��������������ɫ���ٷ����仯ʱ����Ӧ�����µ�ƽ��
C����Ӧ�ﵽ��ƽ��ʱ��ѹǿ��ԭƽ����ͬ
D����Ӧ�ﵽ��ƽ��ʱ�����������ܶ���ԭƽ�������
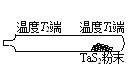
�����á���ѧ����ת�Ʒ��������ᴿ���ѻӷ����ʵ�TaS2��ĩ����Ӧ������ͼ��ʾ��ʯӢ��չ��н��С������¶�ΪT1 ��һ�η���δ�ᴿ��TaS2��ĩ����������I2��g����һ��ʱ������¶�ΪT2 һ�˵õ��˴���TaS2���塣���¶�T1__________T2���������������=�� ����
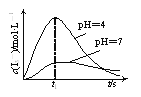
(2)ijʵ��С�����������һ������ͬpHʱO3����ͨ��NaI��Һ�еĹ��̺ͽ���������о���O3ͨ��NaI��Һ�еķ�Ӧ�������£�I3-��Ũ����ʱ��ı仯����ͼ��ʾ��
��Ӧ1��I(aq)��O3(g)=IO(aq)��O2(g)
��Ӧ2��IO(aq)��2H��(aq)��I(aq) ![]() I2(aq)��H2O(l)
I2(aq)��H2O(l)
��Ӧ3��I2(aq)��I(aq) ![]() I3(aq)
I3(aq)
��t1 s֮ǰ��pH��4����Һ�б�pH��7����Һ��I3-��Ũ�ȴ��ԭ����__________��
��t1 s֮����Һ��I3-��Ũ�����½���ԭ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ұ���ķ���������Ϊԭ����ȡ��ϸ��-���������Ƚ��ͻ�����Ⱦ�ֿ��������Դ�������ʡ���֪���ҵ���Ҫ�ɷ�ΪAl2O3������������SiO2��FeO��Fe2O3�������Ʊ�ʵ���������£�
��1�������������������ᷴӦ�Ļ�ѧ����ʽΪ ��
��2����ͼ������������NaOH�����Ʊ������ƣ��ɲ��õ�װ��Ϊ ����ѡ���ţ���

��3����ʵ�������У���30%��H2O2��Һ���������ӷ�Ӧ����ʽΪ ��
��4����֤������������Һ���Ƿ��������ӵIJ�������Ϊ ��
��5�����õ���pH��Һ������������õ�Fe(OH)3����֪��25��ʱ��Ksp[Fe(OH)3]=4.0��10-38������¶��·�ӦFe3++3H2O![]() Fe(OH)3+3H+��ƽ�ⳣ��Ϊ ��
Fe(OH)3+3H+��ƽ�ⳣ��Ϊ ��
��6������������茶��壬��������Ҫ��ӦΪ��4[NH4Al(SO4)2��12H2O]![]() 2Al2O3+ 2NH3��+ N2��+ 5SO3��+ 3SO2��+ 53H2O,������������ͨ����ͼ��ʾ��װ�á�
2Al2O3+ 2NH3��+ N2��+ 5SO3��+ 3SO2��+ 53H2O,������������ͨ����ͼ��ʾ��װ�á�

������ƿ���ռ����������� (�ѧʽ)��
��KMnO4��Һ��ɫ�����������ӷ�Ӧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������ԭ�����͵���( ��
A��H2��I2��HIƽ��������ѹ����ɫ����
B����ҵ���������͵����ϳɰ����ڽϸ��¶��½��е�
C��Fe(SCN��3��Һ�м������KSCN����ɫ����
D��SO2��������SO3�ķ�Ӧ��������Ҫʹ�ô���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���� ![]() ͨ�������KOH��Һ�У������п�����KCl��KClO��
ͨ�������KOH��Һ�У������п�����KCl��KClO��![]() ���Ҳ���ijɷ����¶ȸߵ��йء������й�˵������ȷ����
���Ҳ���ijɷ����¶ȸߵ��йء������й�˵������ȷ����
A.��ij�¶��£���Ӧ��![]() ������Һ��
������Һ��![]()
B.�μӷ�Ӧ��KOH�����ʵ�������![]()
C.�ı��¶ȣ�������![]() ��������۲���Ϊ
��������۲���Ϊ![]()
D.�ı��¶ȣ���Ӧ��ת�Ƶ��ӵ����ʵ���![]() �ķ�Χ��
�ķ�Χ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������巴Ӧ�ﵽ��ѧƽ�⣬ƽ�ⳣ��K��c(A)��c2(B)/[c2(E)��c(F)]������ʱ�����¶��ʵ����ͣ�F��Ũ�����ӣ�����˵����ȷ����( )
A. ����c(A)��c(B)��K����
B. �����¶ȣ�����Ӧ��������
C. �÷�Ӧ���ʱ�Ϊ��ֵ
D. �÷�Ӧ�Ļ�ѧ����ʽΪ2E(g)��F(g)![]() A(g)��2B(g)
A(g)��2B(g)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���о����֣����ᷢ��������ԭ��Ӧʱ�������Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�����һ���������ۺ����۵Ļ������һ������ϡ�������ַ�Ӧ����Ӧ������������ų����ڷ�Ӧ���������Һ����μ���![]() ��Һ������NaOH��Һ�����
��Һ������NaOH��Һ�����![]() ��������������ʵ���
��������������ʵ���![]() ��ϵ����ͼ��ʾ������˵������ȷ����
��ϵ����ͼ��ʾ������˵������ȷ���� ![]()
![]()
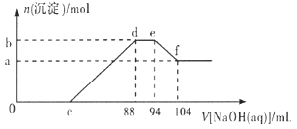
A.ϡ���������ۡ����۷�Ӧ���仹ԭ����Ϊ�����
B.c���Ӧ��Һ�����Ϊ![]()
C.b����a��IJ�ֵΪ![]()
D.��Ʒ�����ۺ����۵����ʵ���֮��Ϊ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��300 ��ʱ����2 mol A��2 mol B������������2 L�ܱ������У��������·�Ӧ��3A(g)��B(g)![]() 2C(g)��2D(g)����H��2 minĩ�ﵽƽ�⣬����0.8 mol D��
2C(g)��2D(g)����H��2 minĩ�ﵽƽ�⣬����0.8 mol D��
��1��300 ��ʱ���÷�Ӧ��ƽ�ⳣ������ʽΪ��K��_______����֪K300 ��<K350 ��������H______0������>������<������
��2����2 minĩʱ��B��ƽ��Ũ��Ϊ_______��D��ƽ����Ӧ����Ϊ_______��
��3�����¶Ȳ��䣬��С�����ݻ�����A��ת����______������������ ����С����������������ԭ����_______��
��4���������ͬ�������£�������Ӧ���淴Ӧ������У���ʼʱ����C��D��4/3 mol����ʹƽ��ʱ�����ʵ����ʵ���Ũ����ԭƽ����ͬ����Ӧ�ü���B_______mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊ��Ҫ�ĺ�������γ��������Ҫ��Ⱦ��֮һ��
��1����ʵ�����У�����70����������Һ���������Ʒ�ĩ��Ӧ��ȡ��������Ҫ����Ʒ�Ӧ���ʣ���ѡ����ͼ��ʾ���巢��װ���е�_____(�����������ĸ)��

��2��SO2��������������SO3���÷�Ӧ���Ȼ�ѧ����ʽΪ��2SO2(g)+O2(g)![]() 2SO3(g) ��H="a" kJ��mol-1����T1��ʱ����2 mol SO2��1mol O2�����ݻ�Ϊ2 L���ܱ�����A�У���ַ�Ӧ���ﵽƽ�⣬�˹����зų�����98��3 kJ�����SO2��ƽ��ת����Ϊ50������a=_____��T1��ʱ��������Ӧ��ƽ�ⳣ��K1=____L��mol-1��������ʼ�¶�ΪT1����2 mol SO2��1 molO2�����ݻ�Ϊ2 L�ľ����ܱ�����B�У���ַ�Ӧ����T2��ʱ�ﵽƽ�⣬�ڴ��¶�ʱ������Ӧ��ƽ�ⳣ��ΪK2����K1______K2(����>������<������=��)��
2SO3(g) ��H="a" kJ��mol-1����T1��ʱ����2 mol SO2��1mol O2�����ݻ�Ϊ2 L���ܱ�����A�У���ַ�Ӧ���ﵽƽ�⣬�˹����зų�����98��3 kJ�����SO2��ƽ��ת����Ϊ50������a=_____��T1��ʱ��������Ӧ��ƽ�ⳣ��K1=____L��mol-1��������ʼ�¶�ΪT1����2 mol SO2��1 molO2�����ݻ�Ϊ2 L�ľ����ܱ�����B�У���ַ�Ӧ����T2��ʱ�ﵽƽ�⣬�ڴ��¶�ʱ������Ӧ��ƽ�ⳣ��ΪK2����K1______K2(����>������<������=��)��
��3��ij�ȵ糧�Ͽմ��������������������س��꣬�ֶԸ�������ˮ��Ʒ����̽����������pH��ֽ�ⶨ��ˮ��Ʒ��pH����������Ϊ___________________________�������ƷpHԼΪ3��Ϊ��һ��̽����SO3���γ���������ʣ���һ������SO2ͨ������ˮ�У����pHΪ3����Һ��Ȼ����Һ��ΪA��B���ݣ���A�м���������NaOH���壬ʹ��Һǡ�ó�����(���������������ʺ������������ʵ�Ӱ��)�����������Һ�����ӵ�Ũ�ȼ���ڵĹ�ϵʽΪ��[Na+]=______________������ҺB�����ڿ����У������ǰ��ȣ����ú����ҺB��ˮ�ĵ���̶Ƚ�__________(����������������С������������)��
��4����ҵ�ϳ�������ͼ��ʾ�����̴�����ҵβ���е�SO2��

������������һ�����ʿ�������ѭ�����ã������������Ļ�ѧ����ʽΪ_______________.
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com