
| A. | 密闭容器中,2mol SO2和1mol O2充分反应,生成SO3的分子数为2 NA | |
| B. | 1L1 mol•L-1 的(NH4)2SO4 溶液中含有的 NH4+数目为2NA | |
| C. | 足量的 MnO2与 100ml 12 mol•L-1的浓盐酸充分反应,转移的电子数目为 0.6 NA | |
| D. | 常温常压下,18 mL 水含有的分子数目约为 NA |
分析 A.二氧化硫与氧气反应为可逆反应;
B.氨根离子为弱碱阳离子,水溶液中部分水解;
C.稀盐酸与二氧化锰不反应;
D.18 mL 水质量为18g,依据n=$\frac{m}{M}$=$\frac{N}{N{\;}_{A}}$计算.
解答 解:A.二氧化硫与氧气反应为可逆反应,可逆反应不能进行到底,所以2mol SO2和1mol O2充分反应,生成SO3的分子数小于2 NA,故A错误;
B.氨根离子为弱碱阳离子,水溶液中部分水解,所以1L1 mol•L-1 的(NH4)2SO4 溶液中含有的 NH4+数目小于2NA,故B错误;
C.足量的 MnO2与 100ml 12 mol•L-1的浓盐酸充分反应,随着反应进行盐酸浓度降低变为稀盐酸,稀盐酸不二氧化锰不反应,所以转移的电子数目小于 0.6 NA,故C错误;
D.常温常压下,18 mL 水质量为18g,物质的量为$\frac{18g}{18g/mol}$=1mol含有的分子数目约为 NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,明确盐类水解的性质、可逆反应特点、二氧化锰与浓盐酸反应条件,题目难度中等.


科目:高中化学 来源: 题型:选择题
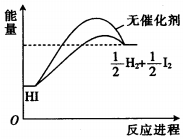
| A. | 加入催化剂,减小了反应的活化能 | |
| B. | 加入催化剂,可提高HI的平衡转化率 | |
| C. | 降低温度,HI的分解速率加快 | |
| D. | 反应物的总能量大于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铁胶体可用于净水 | B. | Fe2O3可用作红色涂料 | ||
| C. | 纯碱溶液可用于去除油污 | D. | MnO2和浓HCl可用于工业制氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
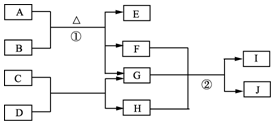 有关物质的转化关系如图1所示.A是黑色非金属单质,C、E、F均为氧化物,E、F常温下呈气态,且E能使品红褪色,G是一种常见的无色液体,I是一种难溶于水的白色胶状沉淀,能溶于B溶液.请回答下列问题:
有关物质的转化关系如图1所示.A是黑色非金属单质,C、E、F均为氧化物,E、F常温下呈气态,且E能使品红褪色,G是一种常见的无色液体,I是一种难溶于水的白色胶状沉淀,能溶于B溶液.请回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化钠溶液加入稀硝酸:S2-+2H+═H2 S↑ | |
| B. | 用惰性电极电解饱和硫酸铜溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | NaHSO4溶液与Ba(OH)2溶液混合:HSO4-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56g铁片与足量浓H2SO4在加热的条件下可生成1.5NA个SO2分子 | |
| B. | 标准状况下20g D2O分子中所含中子数为10NA | |
| C. | 常温下,将0.1NA个氯化氢分子溶于1L水中,得到0.1mol/L的盐酸 | |
| D. | 2.8g乙烯和2.8g聚乙烯中含碳原子数均为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;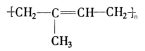 其单体的结构简式CH2=C(CH3)CH=CH2;
其单体的结构简式CH2=C(CH3)CH=CH2;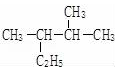 的名称(系统命名法)2,3-二甲基戊烷.
的名称(系统命名法)2,3-二甲基戊烷.查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com