
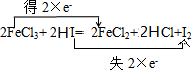 ������0.1mol��Fe2+����ʱ��ת�Ƶ�����ĿΪ0.1NA��
������0.1mol��Fe2+����ʱ��ת�Ƶ�����ĿΪ0.1NA������ ��1����Ӧ����һ�ֵ����û���һ�ֵ��ʣ������û���Ӧ��
��2����Ӧ��Cl2��Cl�õ��ӣ�FeCl2��Feʧ���ӣ�
��3��FeԪ�صĻ��ϼ۽��ͣ�IԪ�صĻ��ϼ����ߣ��÷�Ӧת��2e-��
��4����Ӧ��Cl2+2KI�T2KCl+I2�������Ե��θ�дΪ���ӣ�
��� �⣺��1����Ӧ��H2S+I2�TS+2HI��һ�ֵ����û���һ�ֵ��ʣ������û���Ӧ���÷�Ӧ��S��IԪ�صĻ��ϼ۷����仯������������ԭ��Ӧ��
�ʴ�Ϊ��AD��
��2����Ӧ��2FeCl2+Cl2�T2FeCl3��Cl2��Cl��2�����ӣ�FeCl2��Feʧ1�����ӣ���ԭ���������������ʵ���֮��Ϊ2��1��
�ʴ�Ϊ��2��1��
��3��FeԪ�ػ��ϼ۴�+3�۱仯Ϊ+2�۵õ����ӣ���FeCl3Ϊ����������Ԫ�ػ��ϼ۴�-1�۱仯Ϊ0�ۣ���HIΪ��ԭ������˫���ű�ע����ת��Ϊ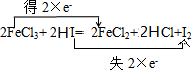 ������0.1mol��Fe2+����ʱ��ת�Ƶ���Ϊ0.1mol��������ĿΪ0.1NA��
������0.1mol��Fe2+����ʱ��ת�Ƶ���Ϊ0.1mol��������ĿΪ0.1NA��
�ʴ�Ϊ��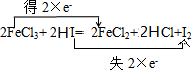 ��0.1NA��
��0.1NA��
��4����Ӧ��Cl2+2KI�T2KCl+I2�������Ե��θ�дΪ���ӣ������ӷ���ʽΪ��Cl2+2I-�TCl-+I2��
�ʴ�Ϊ��Cl2+2I-�TCl-+I2��
���� ���⿼��������ԭ��Ӧ�����շ�Ӧ��Ԫ�صĻ��ϼ۱仯Ϊ���Ĺؼ�������������ԭ��Ӧ�������ת�Ƶ��ӱ�ʾ�����Ŀ��飬��Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | x��ֵΪ1 | B�� | v��B��=0.2mol•L-1•min-1 | ||
| C�� | ��Ӧ��ʼǰA�����ʵ���Ϊ3mol | D�� | 5minʱA��Ũ��Ϊ0.2mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���е����� | ���е����� | ���е����� | ���е����� | 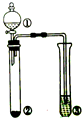 |
| A | Ũ��ˮ | NaOH | AlCl3��Һ | �Ȳ�����ɫ������������ܽ� | |
| B | Ũ���� | MnO2 | KI��Һ | ��Һ����ɫ | |
| C | Ũ���� | Na2SO3 | Ba��NO3��2��Һ | �������� | |
| D | Ũ���� | Cu | ����̪��NaOH��Һ | ��Һ��ɫ��ȥ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������CO��CO2��O3�ֱ���1mol O����������������ʵ���֮��Ϊ3��2��1 | |
| B�� | ng Cl2����m��Clԭ�ӣ����ӵ�����NA����ֵ�ɱ�ʾΪ$\frac{35.5m}{n}$ | |
| C�� | ��״���£�11.2L X������ӵ�����Ϊ16g����X�����Ħ��������32 | |
| D�� | 30g CO��22.4L CO2�к��е�̼ԭ����һ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����2NA����ԭ�ӵĺ����ڱ�״���µ����ԼΪ22.4L | |
| B�� | 25�棬1.01��105 Pa��64g SO2�к��е�Oԭ����Ϊ2NA | |
| C�� | �ڳ��³�ѹ�£�22.4L Cl2���еķ�����ΪNA | |
| D�� | ��״���£�11.2LCH3CH2OH���ƾ������еķ�����Ϊ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com