
“温室效应” 是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。![]()
![]()
![]()
![]()
![]()
![]()
![]()

(1)下列措施中,有利于降低大气中CO2浓度的有 。(填字母)
a.减少化石燃料的使用 b.植树造林,增大植被面积
c.采用节能技术 d.利用太阳能、风能
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
![]()
![]() a.6CO2+6H2O C6H12O6+6O2 b.CO2+3H2 CH3OH+H2O
a.6CO2+6H2O C6H12O6+6O2 b.CO2+3H2 CH3OH+H2O
![]()
![]() c.CO2+CH4 CH3COOH d.2CO2+6H2 CH2=CH2+4H2O
c.CO2+CH4 CH3COOH d.2CO2+6H2 CH2=CH2+4H2O
以上反应中,最节能的是 ,原子利用率最高的是 。
(3)文献报道某课题组利用CO2催化氢化制甲烷的研究过程如下:

反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4。CH4、HCOOH、H2的产量和镍粉用量的关系如下图所示(仅改变镍粉用量,其他条件不变):

研究人员根据实验结果得出结论:HCOOH是CO2转化为CH4的中间体,即:
![]()
![]() CO2 HCOOH CH4
CO2 HCOOH CH4
①写出产生H2的反应方程式 。
 ②由图可知,镍粉是 。(填字母)
②由图可知,镍粉是 。(填字母)
a.反应Ⅰ的催化剂
b.反应Ⅱ的催化剂
c.反应Ⅰ、Ⅱ的催化剂
d.不是催化剂![]()
![]()
![]()
![]()
![]()
![]()
![]()

③当镍粉用量从1 mmol增加到10 mmol,反应速率的变化情况是 。(填字母)
a.反应Ⅰ的速率增加,反应Ⅱ的速率不变
b.反应Ⅰ的速率不变,反应Ⅱ的速率增加
c.反应Ⅰ、Ⅱ的速率均不变
d.反应Ⅰ、Ⅱ的速率均增加,且反应Ⅰ的速率增加得快
e.反应Ⅰ、Ⅱ的速率
均增加,且反应Ⅱ的速率增加得快
f.反应Ⅰ的速率减小,反应Ⅱ的速率增加
(1)abcd (2)a c
![]() (3)①3Fe+4H2O(g) Fe3O4+4H2 ②c ③e
(3)①3Fe+4H2O(g) Fe3O4+4H2 ②c ③e
(1)a、c、d的措施可以减少CO2的产生,而b可以大量消耗CO2,故a、b、c、d都应选。
(2)a不需外加能源,节能;c无副产物,原子利用率最高。
![]() (3)①3Fe+4H2O(g) Fe3O4+4H2
(3)①3Fe+4H2O(g) Fe3O4+4H2
②由图表中看出随镍粉增加H2量迅速减少,说明是反应Ⅰ的催化剂,HCOOH量也迅速减少,说明也是反应Ⅱ的催化剂。
③当镍从1 mmol增加到10 mmol,H2和HCOOH的量仍在减少,说明反应Ⅰ和反应Ⅱ的反应速率都增加,但甲烷的增加量明显快于H2的减少量,说明反应Ⅱ增加得快。


科目:高中化学 来源: 题型:
| 物质 | 大气中的含量 (体积百分比) |
温室效应 指数 |
| CO2 | 0.03 | 1 |
| H2O | 1 | 0.1 |
| CH4 | 2×10-4 | 30 |
| N2O4 | 3×10-5 | 160 |
| O3 | 4×10-6 | 2000 |
| CCl2F2 | 4.8×10-8 | 25000 |
 ,分子为平面结构.N2O4分子中N原子的杂化方式为
,分子为平面结构.N2O4分子中N原子的杂化方式为

| 共价键 | C-C | C-N | C-S |
| 键能/kJ?mol-1 | 347 | 305 | 259 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| △ |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 哥本哈根世界气候大会全称《联合国气候变化框架公约》第15次缔约方会议暨《京都议定书》第5次缔约方会议,于2009年12月7~18日在丹麦首都哥本哈根召开.来自192个国家的谈判代表召开峰会,商讨《京都议定书》一期承诺到期后的后续方案,即2012~2020年的全球减排协议.
哥本哈根世界气候大会全称《联合国气候变化框架公约》第15次缔约方会议暨《京都议定书》第5次缔约方会议,于2009年12月7~18日在丹麦首都哥本哈根召开.来自192个国家的谈判代表召开峰会,商讨《京都议定书》一期承诺到期后的后续方案,即2012~2020年的全球减排协议.| 序号 | 预测现象 | 实验结论 |
| A | ||
| B | ||
| C |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
阅读下列短文,完成以下4题
英国国家海洋学中心于2009年8月14日发布新闻公报说,中心的研究人员及其同行利用声呐等手段探测到北极海洋中存在大量甲烷气泡,证实了全球变暖会使海底释放大量甲烷的说法。研究人员认为,这些甲烷可能会反过来加剧全球变暖。
(1)已知天然气的主要成分CH4是一种会产生温室效应的气体,等物质的量的CH4和CO2产生的温室效应,前者大。下面是有关天然气的几种叙述,其中正确的是( )
①天然气与煤、柴油相比是较清洁的能源;②等质量的CH4和CO2产生的温室效应也是前者大;③燃烧天然气也是酸雨的成因之一
A.①②③ B.只有① C.①和② D.只有③
(2)可燃冰又称天然气水合物,它是海底的高压、低温条件下形成的,外观像冰。其化学式为8CH4·46H2O,1体积可燃冰可贮载100~200体积的天然气。下面关于可燃冰的叙述不正确的是( )
A.可燃冰有可能成为人类未来的重要能源
B.可燃冰是一种比较洁净的能源
C.可燃冰提供了水可能变成油的例证
D.可燃冰的主要可燃成分是甲烷
(3)下列事实、事件、事故中与甲烷无关的是( )
A.天然气的主要成分
B.造成“光化学烟雾”的气体
C.“西气东输”工程
D.煤矿中的瓦斯爆炸
(4)下列叙述中正确的是( )
A.在通常情况下,甲烷与高锰酸钾等强氧化剂不反应,与强酸、强碱也不反应
B.甲烷燃烧能放出大量的热,所以它是一种很好的气体燃料,但点燃甲烷不必像点燃氢气那样事先验纯
C.甲烷分子是空间正方体结构,甲烷分子中4个碳氢键是完全等同的
D.1 mol CH4与4mol Cl2发生取代反应后,测得四种有机取代物的物质的量相等
查看答案和解析>>
科目:高中化学 来源:2010年银川二中高考预测(综合题)化学卷 题型:实验题
运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)CO2是一种重要的物质,但其过量排放,可能导致全球气温升高。下列措施不能够有效控制CO2所导致的温室效应的是_________(填序号)
①大力发展低碳产业,提倡低碳生活,依法控制CO2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka =4.7×10-8。写出84消毒液露置在空气中发生反应的离子方程式___________________________。
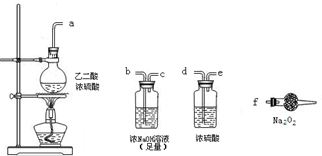
(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应。
已知: ,则实验选择的最简单的装置接口连接顺序为________;
,则实验选择的最简单的装置接口连接顺序为________;
若CO能够与Na2O2发生反应,则预测反应产物为____________。实验后用球形干燥管中的固体进行验证可选择的试剂是_______________________________。
(4)已知C(s)+O2(g)=CO2(g),△H="-393.5" kJ·mol -1 ;CO(g)+ O2(g)=CO2(g),△H="-283.0" kJ·mol -1,写出CO2和C(s)反应的热化学方程式___________________。以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为______________________。若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)________L。
O2(g)=CO2(g),△H="-283.0" kJ·mol -1,写出CO2和C(s)反应的热化学方程式___________________。以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为______________________。若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com