
分析 (1)甲方案中Cu与浓硫酸加热反应生成硫酸铜、二氧化硫和水;
(2)甲中生成有毒气体二氧化硫,乙中操作复杂且生成有毒气体,只有丙中不生成有毒气体;
(3)n(HNO3)=0.2mol,n(H2SO4)=0.4mol,则n(H+)=1.0mol,结合3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O及Cu~CuSO4•5H2O结合计算;
(4)高温灼烧固体应在坩埚中进行;溶液通过蒸发、结晶得到硫酸铜晶体;
(5)由反应物及产物可知,X具有氧化性,结合元素守恒可知X为H2O2,反应生成硫酸铜和水.
解答 解:(1)甲方案中Cu与浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)甲中生成有毒气体二氧化硫,乙中操作复杂且生成有毒气体,只有丙中总反应为2Cu+O2+2H2SO4═2CuSO4+2H2O,不生成有毒气体,则丙方案合理,
故答案为:丙;不排放有毒气体;
(3)n(HNO3)=0.2mol,n(H2SO4)=0.4mol,则n(H+)=1.0mol,由3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O可知,硝酸完全反应生成的铜离子为0.3mol,由Cu~CuSO4•5H2O可知,CuSO4•5H2O的质量为0.3mol×250g/mol=75g,
故答案为:75g;
(4)高温灼烧固体应在坩埚中进行,因此仪器应为坩埚;溶液通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到硫酸铜晶体,
故答案为:坩埚;蒸发浓缩、冷却结晶、过滤、洗涤、干燥;
(4)由反应物及产物可知,X具有氧化性,结合元素守恒可知X为H2O2,铜与双氧水、硫酸反应生成硫酸铜,化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O,
故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O.
点评 本题考查物质的制备实验及评价,为高频考点,把握物质的性质、制备实验原理及实验评价为解答的关键,侧重分析与实验能力的考查,注意发生的氧化还原反应及应用,题目难度中等.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:选择题
| A. | 丁烷的结构简式为:CH3CH2CH2CH2CH3 | |
| B. | 甲醛的电子式为: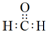 | |
| C. | 有机物CH2═CH-CH2-CH3的键线式为: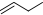 | |
| D. | 乙酸(CH3COOH)的最简式为:C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
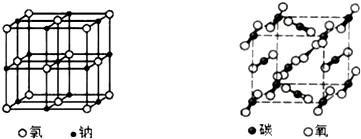
| A. | 两种晶体内均含有共价键 | B. | 构成两种晶体的微粒均是原子 | ||
| C. | 两者的硬度、熔沸点差别较大 | D. | 两种晶体均属于离子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
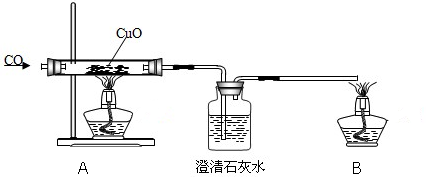
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,180g淀粉水解得到葡萄糖的分子数为NA | |
| B. | 1 mol C10H22分子中共价键总数为31 NA | |
| C. | 室温下,4.4 g乙醛和乙酸乙酯的混合物含有的碳原子数为0.2 NA | |
| D. | 88.0g干冰中含有的共用电子对对数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SiO3 H2S CO2 | B. | H2O NH3•H2O H3PO4 | ||
| C. | H2SO3 BaSO4 CH4 | D. | MgSO4 CH3COOH CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
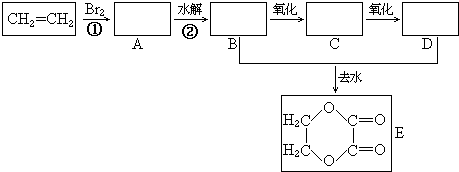
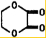 +2H2O.
+2H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com