
在恒温、容积为2L的密闭容器中充入2mol SO2和一定量O2。发生反应2SO2+O2 2SO3,当反应进行到4min时,测得n(SO2)=0.4mol。若反应进行到2min时,容器中SO2的物质的量是
2SO3,当反应进行到4min时,测得n(SO2)=0.4mol。若反应进行到2min时,容器中SO2的物质的量是
A.等于1.6 mol B.等于1.2 mol C.大于1.6 mol D.小于1.2 mol
科目:高中化学 来源:2015-2016学年甘肃省白银市高二上期中文化学卷 (解析版) 题型:选择题
下列说法中不正确的是( )
A.人体缺碘,可通过食用加碘盐补碘
B.缺铁性贫血,可通过食用铁强化酱油预防
C.为了防止龋齿,人人都要使用含氟牙膏
D.儿童缺锌可导致生长发育不良,抵抗力差,食欲不振
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学试卷(解析版) 题型:选择题
 是常规核裂变产物之一,可以通过测定大气或水中
是常规核裂变产物之一,可以通过测定大气或水中 的含量变化来检测核电站是否发生放射性物质泄漏。下列有关
的含量变化来检测核电站是否发生放射性物质泄漏。下列有关 的叙述中正确的是
的叙述中正确的是
A.  的原子核内中子数多于质子数 B.
的原子核内中子数多于质子数 B.  的原子序数为131
的原子序数为131
C.  的原子核外电子数为78 D.
的原子核外电子数为78 D.  的化学性质与
的化学性质与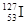 不同
不同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
下列事实中,不能用勒夏特列原理解释的是
A.冰镇的啤酒打开后泛起泡沫
B.由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
C.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
D.黄绿色的氯水光照后颜色变浅
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高二上期中化学试卷(解析版) 题型:选择题
已知:
2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1452 kJ·mol-1
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
下列说法正确的是:
A.H2(g)的燃烧热为571.6 kJ·mol-1
B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C.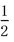 H2SO4(aq)+
H2SO4(aq)+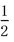 Ba(OH)2(aq)=
Ba(OH)2(aq)=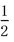 BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D.3H2(g)+CO2(g)=CH3OH(l)+H 2O(l) ΔH=+135.9 kJ·mol-1
2O(l) ΔH=+135.9 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上10月月考化学卷(解析版) 题型:填空题
CH3OH是一种重要的化工原料,工业上可用合成气(CO和H2)来生产,主要副产物有CH4、C2H5OH等。已知生产CH3OH和副产物CH4的热化学方程式分别为
①CO(g)+2H2(g) CH3OH(g) △H=-90.7 kJ·mol-1
CH3OH(g) △H=-90.7 kJ·mol-1
②CO(g)+ 3H2(g) CH4(g)+H2O(g) △H=-206.2 kJ·mol-1
CH4(g)+H2O(g) △H=-206.2 kJ·mol-1
回答下面问题
(1)若CO(g)和CH3OH(g)的燃烧热△H分别为-283 kJ·mol-1和-726.1 kJ·mol-1,则H2(g)的燃烧热△H为 。
(2)下表列出了几种化学键断裂需要的能量数据。
化学键 | C≡O | H-H | C-H | H-O |
断裂1mol需要能量 / kJ | a | 436 | 414 | 463 |
则a= 。
(3)工业生产CH3OH过程中,提高合成CH3OH反应选择性的关键因素是 。
(4)下表列出了在一定条件下,在 3个1L容器中发生反应①时测得的一些数据。
3个1L容器中发生反应①时测得的一些数据。
容器序号 | 温度 / ℃ | 物质的起始浓度 / mol·L-1 | 物质平衡时浓度/ mol·L-1 | ||
H2 | CO | CH3OH | CH3OH | ||
Ⅰ | 100 | 0.2 | 0.1 | 0 | 0.02 |
Ⅱ | 100 | 0.4 | 0.2 | 0.1 | |
Ⅲ | 200 | 0 | 0 | 0.10 | b |
① CO(g)+2H2(g) CH3OH(g)的平衡常数表达式为 ;
CH3OH(g)的平衡常数表达式为 ;
② 容器Ⅱ中,开始时,v(正) v(逆) (填“<、>、=”) ;
③ 容器Ⅲ中,达平衡时 b 0.02(填“<、>、=”) ;
④ 达到平衡时,正反应速率:容器Ⅲ中的比容器Ⅰ中的 (填“大、小、相等”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上10月月考化学卷(解析版) 题型:选择题
在一定温度下,反应H2(g)+ X2(g) 2HX(g)的平衡常数为100。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
2HX(g)的平衡常数为100。若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
A.5% B.17% C.25% D.33%
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上第二次月考化学卷(解析版) 题型:实验题
下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
【实验目的】制取乙酸乙酯
【装置设计】甲、乙、丙三位同学分别设计了下列三套实验装置:
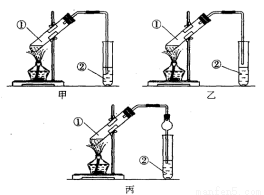
请从甲、乙两位同学设计的装置中选择一种作为实验室制取乙酸乙酯的装置,我选择的装置是 (选填 “甲”或 “乙”)。丙同学将甲装置中的玻璃管改成了球形干燥管除起冷凝作用外,它的另一重要作用是 。
【问题讨论】
a.根据试管②中观察到的现象,可知乙酸乙酯的物理性质有:
无色油状液体、 、 ;
b.试管②中饱和 Na2CO3 溶液的作用是 (填编号)。
A.溶解乙醇 B.降低乙酸乙酯的溶解度 C.中和乙酸
c.从试管②中分离出乙酸乙酯的实验操作是 。
d.生成乙酸乙酯的化学反应方程式 。
f.乙醇在铜或银作催化剂时,可以被氧化为一种有刺激性气味的物质,写出该反应的化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上第二次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A? SO3溶于水能导电,所以SO3是电解质
B? 凡是元素化合价发生了改变的反应,都是氧化还原反应
C? 酸、碱、盐是电解质,都有很强的导电能力
D? 酸和碱之间的中和反应不一定非氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com