
2014 年 3 月 21 日是第二十二届“世界水日”,保护水资源,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂。当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的____________倍。
2)某无色废水中可能含有 Fe3+、Al3+、Mg2+、Na+、NO-、CO32-、SO42-离子中的几种,为分析其成分,分别取废水样品 100 mL,进行了三组实验,其操作和有关现象如下图所示:
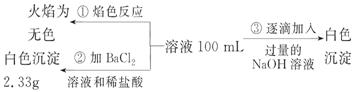
请根据上图回答下列问题:
①实验中需配制 1.0 mol/L的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管, 还缺少的仪器为_________。
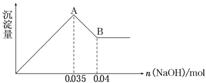
②实验③中沉淀量由 A→B过程中所发生反应的离子方程式为__________。
③试确定NO3-是否存在?_______(填“存在”、“不存在”或“不确定”),若存在,试计算 c(NO3-)=____________(若不存在,此问不必作答)。
【知识点】元素化合物、离子推断A3 B1 D5 C5
【答案解析】(1)2.5
(2)①100mL容量瓶 ②Al(OH)3+OH-=AlO2-+2H2O ③存在 0.15mol/L
解析:⑴消耗1mol ClO2得到电子5mol、消耗1molCl2得到电子2mol,ClO2的消毒效率是Cl2的2.5倍⑵根据废水无色知无Fe3+,根据焰色反应呈无色知没有Na+,根据实验②产生白色沉淀知有SO42-,而且其物质的量为2.33/233=0.01mol,根据实验③确定有Al3+和Mg2+,因为CO32-与Al3+不能共存,所以无CO32-,因此溶液中存在的离子为:Al3+、Mg2+、SO42-,根据图象可知Al(OH)3的物质的量为0.005mol,溶解氢氧化铝消耗OH-为0.005mol,生成氢氧化铝沉淀消耗OH-为0.015mol,则生成氢氧化镁沉淀消耗OH-为0.035mol-0.015mol=0.02mol,则Mg2+为0.01mol,根据电荷守恒知NO3-的物质的量为0.005×3+0.01×2-0.01×2=0.015mol,c(NO3-)=0.15mol/L;A→B段的反应是氢氧化铝的溶解Al(OH)3+OH-=AlO2-+2H2O;配制 1.0 mol/L的NaOH溶液100 mL还需100mL容量瓶。
【思路点拨】根据离子共存和实验现象分析判断离子组成;根据物质发生的反应及图像的起点、转折点、终点和曲线变化的意义进行分析计算。


 精英口算卡系列答案
精英口算卡系列答案科目:高中化学 来源: 题型:
天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、S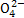 、Br-、C
、Br-、C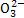 、HC
、HC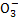 等离子,火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:
等离子,火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:
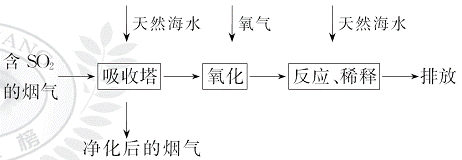
下列说法错误的是( )
A.天然海水pH≈8的原因是海水中的C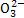 、HC
、HC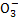 水解
水解
B.“氧化”是利用氧气将HS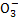 、S
、S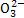 等氧化生成S
等氧化生成S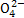
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸
D.“排放”出来的海水中S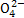 的物质的量浓度与进入吸收塔的天然海水相同
的物质的量浓度与进入吸收塔的天然海水相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定溶液中能大量共存的是
A.常温下,c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+
B.某溶液中可能大量存在:Fe3+、K+、HCO3-、SO42-
C.使pH试纸变蓝的溶液中:NH4+、Na+、SO42-、Cl-
D.酸性溶液中:K+、Al3+、I-、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性溶液X含有Ba2+、Al3+、NH 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO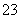 、SO
、SO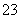 、SO
、SO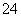 、Cl-、NO
、Cl-、NO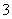 中的一种或几种,取该溶液进行实验,实验内容如下:
中的一种或几种,取该溶液进行实验,实验内容如下:
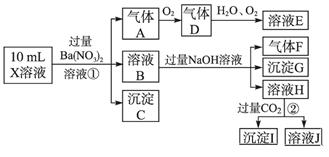
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是_____________________________________;
(2)写出有关离子方程式:
步骤①中生成A__________________;步骤②生成沉淀I__________________。
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,而沉淀C物质的量0.07 mol,能说明该溶液不能确定的阴离子存在的理由是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
钾水玻璃以其优异的性能广泛用于防腐、铸造、油田、钻井或各种高档涂料中。钾水玻璃中硅含量的测定可以采用氟硅酸钾容量法,其步骤为:
①称取试样溶解在含有过量的氟离子和钾离子的强酸溶液中,硅能与氟离子、钾离子作用生成氟硅酸钾(K2SiF6)沉淀;
②沉淀分离后于热水中水解,生成HF、H2SiO3、KF;
③过滤除去硅酸沉淀,用氢氧化钠标准溶液滴定滤液。
(1)上述步骤②中的水解反应方程式为 ;
步骤③中反应的离子方程式为: 。
(2)在步骤③中,若滴定前未用氢氧化钠标准溶液润洗滴定管,则测得的硅元素含量将
(填“偏高”、或“偏低”或“不变”)。
(3)若每次称取试样的质量为1.00g,重复滴定四次,消耗1.00 mol·L-1氢氧化钠标准溶液的体积为分别为16.80mL、19.90mL、20.00mL、20.10mL,试计算该试样中硅元素的质量分数(以二氧化硅计),写出计算过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中,不属于同分异构体的是( )
A.乙苯和二甲苯
B.CH2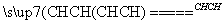 CH2和CH3CCCH3
CH2和CH3CCCH3
C.CH3CH2CH3和CH3(CH2)3CH3
D.CH3CH2OH和CH3OCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
偏二甲肼与N2O4 是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 (l )+2N2O4 (l )=2CO2 (g )+3N2 (g )+4H2O (l ) (Ⅰ)
(1)若将反应(Ⅰ)设计成原电池,则正极的电极反应式为
(酸性电解质)。
(2)火箭残骸中常现红棕色气体,原因为:N2O4 (g) 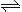 2NO2 (g) (Ⅱ)
2NO2 (g) (Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为 (填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4 充入一恒压密闭容器中,
下列示意图正确且能说明反应达到平衡状态的是________.
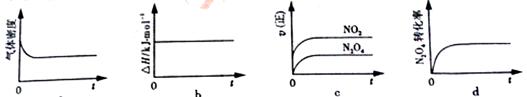
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数________(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=________mol·L-1·s-1。
(4)NO2可用氨水吸收生成NH4NO3 。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是 (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将______(填“正向”“不”或
“逆向”)移动,所滴加氨水的浓度为_______mol·L-1。(NH3·H2O的电离平衡常数
Kb=2×10—5 mol·L-1)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com