
| H+ |
| ��ת�� |
| Fe2+ |
| �ڻ�ԭ |
| OH- |
| �۳��� |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ı�ȼ���ȡ�H=-890.3 kJ?mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890.3 kJ?mol-1 |
B����ϩ�ļ���ʽ��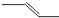 |
| C��һ�������£�ij�ܱ������г���2mol SO2��g����1molO2��g�����ﵽƽ��ų�QkJ��������������µ��Ȼ�ѧ����ʽΪ��2SO2��g��+O2��g��?2SO3��g ����H=-Q kJ?mol-1 |
| D����ϩ�Ľṹ��ʽ��CH2CH2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| A��H2��ȼ����Ϊ-241.8kJ |
| B��2H2��g��+O2��g��=2H2O��g������H=-483.6kJ/mol |
| C��1molH2��ȫȼ������Һ̬ˮ�ų�����������241.8kJ |
| D���Ͽ�1molH2O�Ļ�ѧ�����յ����������ڶ���1molH2��0.5 molO2�Ļ�ѧ�������յ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��25mL 3 mol?L-1��KCl |
| B��75 mL 1.5 mol?L-1��CaCl2 |
| C��150 mL 1 mol?L-1��NaCl |
| D��100 mL 2 mol?L-1��FeCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| P1 | P2 | P3 | |
| T1 | 0.10 | 0.04 | 0.02 |
| T2 | 0.20 | 0.16 | 0.05 |
| T3 | 0.40 | 0.35 | 0.20 |
| c(HCO3) | ||
c(C
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | 1 | 2 | 3 |
| ���������/g | 4.36 | 5.54 | 9.81 |
| ������Һ���/mL | 50.00 | 50.00 | 50.00 |
| ����SO2�����ʵ���/mol | 0.03 | 0.0375 | 0.03 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com