
���� ��1����A��D��ˮ��Һ����ʹʪ�����ɫʯ����ֽ��죬˵����Һ�����ԣ�B�ڳ���ʱΪ���壬��AΪH2S��BΪSO2��CΪSO3��DΪH2SO4��
��2����A��ˮ��Һ��ʹʪ��ĺ�ɫʯ����ֽ��������A��NH3��D��ϡ��Һ��ʹʪ�����ɫʯ����ֽ��죬Ϊ�ᣬ��������������NO��NO��������������NO2������B��NO��C��NO2��D��HNO3��
��3����AΪ���ý���Ԫ�صĵ��ʣ�DΪǿ���ɫ��Ӧ�Ի�ɫ����AΪNa��BΪNa2O��CΪNa2O2����DΪNaOH��
��� �⣺��1����A��D��ˮ��Һ����ʹʪ�����ɫʯ����ֽ��죬˵����Һ�����ԣ�B�ڳ���ʱΪ���壬��AΪH2S��BΪSO2��CΪSO3��DΪH2SO4��B��Cת���Ļ�ѧ��Ӧ����ʽ��2SO2+O2$\stackrel{������}{?}$2SO3��
�ʴ�Ϊ��H2S��2SO2+O2$\stackrel{������}{?}$2SO3��
��2����A��ˮ��Һ��ʹʪ��ĺ�ɫʯ����ֽ��������A��NH3��D��ϡ��Һ��ʹʪ�����ɫʯ����ֽ��죬Ϊ�ᣬ��������������NO��NO��������������NO2������B��NO��C��NO2��D��HNO3��
��A�Ļ�ѧʽΪ��NH3��ʵ�����Ʊ�����A�Ļ�ѧ��Ӧ����ʽΪ��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$2NH3��+CaCl2+2H2O��A��Bת���Ļ�ѧ����ʽΪ��4NH3+5O2$\frac{\underline{����}}{��}$NO+6H2O��
�ʴ�Ϊ��NH3��2NH4Cl+Ca��OH��2$\frac{\underline{\;\;��\;\;}}{\;}$2NH3��+CaCl2+2H2O��4NH3+5O2$\frac{\underline{����}}{��}$NO+6H2O��
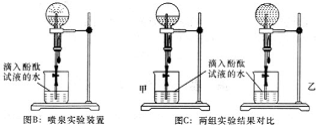
�ڸ���ͼB��Ȫʵ���װ�ý���ʵ�飬�ܹ۲쵽�����ĺ�ɫ��Ȫ���÷���ʽ������Ȫ�ʺ�ɫ��ԭ��NH3+H2O?NH3��H2O?NH4++OH-��
�ʴ�Ϊ��NH3+H2O?NH3��H2O?NH4++OH-��
����Һ������ڰ��������������ͬѧ������Һ�����ʵ���Ũ�ȵ�������ͬѧ������Һ�����ʵ���Ũ�ȣ�
�ʴ�Ϊ�����ڣ�
��3����AΪ���ý���Ԫ�صĵ��ʣ�DΪǿ���ɫ��Ӧ�Ի�ɫ����AΪNa��BΪNa2O��CΪNa2O2����DΪNaOH�����������������̼������Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2CO2=2Na2CO3+O2������������ˮ������Ӧ�����ӷ���ʽΪ��2Na2O2+2H2O=4Na++4OH-+O2����
�ʴ�Ϊ��Na2O��2Na2O2+2CO2=2Na2CO3+O2����2Na2O2+2H2O=4Na++4OH-+O2����
���� ���⿼�������ƶϣ��������ʵ���ɫ�����ʵ����ʽ����ƶϣ�����������ѧ����������Ӧ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| N2Ũ��mol•L-1 | 4.00 | 3.70 | 3.50 | 3.36 | 3.26 | 3.18 | 3.10 | 3.00 | 3.00 | 3.00 |
| COŨ��/mol•L-1 | 0.00 | 0.90 | 1.50 | 1.92 | 2.22 | 2.46 | 2.70 | - | - | - |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢ� | B�� | �ڢ� | C�� | �٢ڢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | SiO2��CO2���ƣ���һ����ԭ�Ӻ�������ԭ�ӹ���һ��SiO2���� | |
| B�� | ������һ�㲻����ˮ������ˮ�ࡢ�մɡ���������Ҫ�ɷ� | |
| C�� | SiO2������������ܺͼӦ�����ܺ��ᷴӦ | |
| D�� | ��Ԫ���ǹ��ɿ�����ʯ����Ҫ�ɷ�֮һ���仯��̬����ȫ��������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �μ�����ʱ���Ȳ����������ܽ� | |
| B�� | ��������Ĥ | |
| C�� | ���ȡ����ɡ����գ����ն���Fe2O3���� | |
| D�� | ���ж����ЧӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��NH3����=2v��CO2���� | B�� | �ܱ���������ѹǿ���� | ||
| C�� | �ܱ������а���������������� | D�� | �ܱ������л��������ܶȲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ����� | ���� | ���� |
| A | �ֱ����Na2CO3��NaHCO3���� | �Թ��ڱڶ���ˮ�� | �������ʾ����ȷֽ� |
| B | ����ʢ��NH4Cl������Թ� | �Թܵײ�������ʧ���Թܿ��о������ᣮ | NH4Cl����������� |
| C | ��I-����ɫ��Һ�еμ�����������ˮ���ٵμӵ�����Һ | ������ۺ���Һ�����ɫ | �����ԣ�Cl2��I2 |
| D | ��FeSO4��Һ���ȵ���KSCN��Һ�ٵμ�H2O2��Һ | ����H2O2����Һ���Ѫ��ɫ | Fe2+�������������л�ԭ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com