
【题目】碳是一种常见的元素,它以多种形式广泛存在于自然界之中。
(1)星际空间存在多种有机分子和无机分子,多数都含有碳元素,C2是一种星际分子,C2和C60互为_______________。
(2)CO2是碳元素重要的氧化物,回答下列有关问题:
①利用CO2与Na2O2反应,可向呼吸面具中提供氧气,其反应方程式为_________________。
②工业上可由CO2和NH3在一定条件下合成尿素,反应方程式为2NH3+CO2![]() CO(NH2)2+H2O当
CO(NH2)2+H2O当![]() 时,CO2的转化率随时间的变化关系如图所示.
时,CO2的转化率随时间的变化关系如图所示.
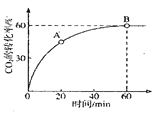
A点的逆反应速率![]() __________B点的正反应速率
__________B点的正反应速率![]() (填“大于“小于”或“等于”),NH3的平衡转化率为____________。
(填“大于“小于”或“等于”),NH3的平衡转化率为____________。
③随着对环境问题认识的深入,CO2的转化捕获问题已成为科研热点之一,以附着纳米银的惰性电极作阴极,可电解CO2转化为CO,装置示意图如下:
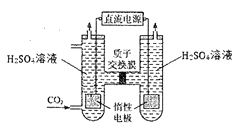
写出通CO2侧电极反应式_________________。
④CO2可用于生产碳酸饮料。苯甲酸钠(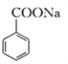 可写为C6H5COONa)也是某些饮料的添加剂,具有抑菌防腐的作用。研究表明苯甲酸(C6H5COOH)的抑菌能力显著高于苯甲酸钠。在生产的某饮料的过程中,除了添加苯甲酸钠外,还需加压充入CO2气体。若忽略碳酸的二级电离,试写出碳酸与苯甲酸钠反应的离子方程式__________________,经计算该反应的化学平衡常数为______________,加压充入CO2后,该饮料的抑菌能力明显增强,结合上述离子方程式分析其原因_______________(已知:H2CO3的Ka1=4.17×10-7;C6H5COOH的Ka=6.25×10-5。)。
可写为C6H5COONa)也是某些饮料的添加剂,具有抑菌防腐的作用。研究表明苯甲酸(C6H5COOH)的抑菌能力显著高于苯甲酸钠。在生产的某饮料的过程中,除了添加苯甲酸钠外,还需加压充入CO2气体。若忽略碳酸的二级电离,试写出碳酸与苯甲酸钠反应的离子方程式__________________,经计算该反应的化学平衡常数为______________,加压充入CO2后,该饮料的抑菌能力明显增强,结合上述离子方程式分析其原因_______________(已知:H2CO3的Ka1=4.17×10-7;C6H5COOH的Ka=6.25×10-5。)。
【答案】 同素异形体 2Na2O2+2CO2=2Na2CO3+O2 小于 30% CO2 +2H+ +2e- =CO +H2O H2CO3 +C6H5COO- ![]() HCO3- + C6H5COOH 6.67×10-3 (6.672×10-3) 加压充入二氧化碳后,碳酸浓度增大平衡向正向移动(反应向正向进行),C6H5COOH浓度增大(或生成了C6H5COOH),抑菌能力增强
HCO3- + C6H5COOH 6.67×10-3 (6.672×10-3) 加压充入二氧化碳后,碳酸浓度增大平衡向正向移动(反应向正向进行),C6H5COOH浓度增大(或生成了C6H5COOH),抑菌能力增强
【解析】(1)C2和C60都是碳的同素异形体,所以C2和C60互为同素异形体;答案为:同素异形体。
(2)①CO2与Na2O2反应,方程式为:2Na2O2+2CO2=2Na2CO3+O2;答案为:2Na2O2+2CO2=2Na2CO3+O2 ②B点反应达到平衡,B点的正反应速率![]() 等于B点的逆反应速率
等于B点的逆反应速率![]() ,A点时生成物的浓度低于B点的浓度所以A点的逆反应速率
,A点时生成物的浓度低于B点的浓度所以A点的逆反应速率![]() 小于B点的逆反应速率
小于B点的逆反应速率![]() ,也就是小于B点的正反应速率
,也就是小于B点的正反应速率![]() ;设氨气的物质的量为4mol,则二氧化碳的物质的量为1mol,平衡时消耗的二氧化碳为1×60%=0.6
;设氨气的物质的量为4mol,则二氧化碳的物质的量为1mol,平衡时消耗的二氧化碳为1×60%=0.6
2NH3+CO2![]() CO(NH2)2+H2O
CO(NH2)2+H2O
初始量(mol)4 1 0 0
转化量(mol)1.2 0.6 氨气的转化率=![]() ×100%=30%
×100%=30%
答案为:小于 30%
③CO2转化为CO,碳的化合价由+4价降为+2价,则通CO2的一极为阴极,发生的电极反应为:CO2 +2H+ +2e- =CO +H2O;答案为:CO2 +2H+ +2e- =CO +H2O
④由电离平衡常数可知C6H5COOH的酸性强于H2CO3,所以忽略碳酸的二级电离,碳酸与苯甲酸钠反应的离子方程式:H2CO3 + C6H5COO- ![]() HCO3- + C6H5COOH,Ka=c(HCO3-)
HCO3- + C6H5COOH,Ka=c(HCO3-)![]() c(C6H5COOH)/c(C6H5COO-)
c(C6H5COOH)/c(C6H5COO-)![]() c(H2CO3)=Ka(H2CO3)/ka(C6H5COOH)=
c(H2CO3)=Ka(H2CO3)/ka(C6H5COOH)= ![]() =6.67×10-3 苯甲酸钠存在水解平衡,溶液显碱性,通入二氧化碳,促进水解,水解生成更多的苯甲酸,抑菌能量增强。答案为:H2CO3 +C6H5COO-
=6.67×10-3 苯甲酸钠存在水解平衡,溶液显碱性,通入二氧化碳,促进水解,水解生成更多的苯甲酸,抑菌能量增强。答案为:H2CO3 +C6H5COO- ![]() HCO3- + C6H5COOH 6.67×10-3(6.672×10-3) 加压充入二氧化碳后,碳酸浓度增大平衡向正向移动(反应向正向进行),C6H5COOH浓度增大(或生成了C6H5COOH),抑菌能力增强
HCO3- + C6H5COOH 6.67×10-3(6.672×10-3) 加压充入二氧化碳后,碳酸浓度增大平衡向正向移动(反应向正向进行),C6H5COOH浓度增大(或生成了C6H5COOH),抑菌能力增强


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( ) 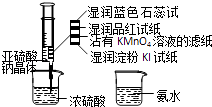
A.蓝色石蕊试纸先变红后褪色
B.品红试纸、沾有KMnO4溶液滤纸均褪色证明了SO2漂白性
C.湿润淀粉KI试纸未变蓝说明SO2的氧化性弱于I2
D.饱和NaCl溶液可用于除去实验中多余的SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油化学工业最重要的基础原料,用乙烯可以制得许多工业材料和日用品,乙烯能发生下列转化关系: 
(1)反应①的化学方程式为:该反应属于反应.
(2)B中所含官能团的电子式为 , D中官能团的名称为 .
(3)已知氯乙烯不溶于水.沸点为﹣13.9℃,则反应②产物A分离的方法为;聚氯乙烯(PVC)曾是世界上产量最大的通用塑料,应用非常广泛.关于聚氯乙烯的说法正确的是 . A.属于纯净物 B.可以燃烧 C.能使溴水褪色 D.可用作食品保鲜膜.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片与稀硫酸的反应B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的碳与二氧化碳的反应D.甲烷在氧气中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】S2Cl2是一种易挥发的液体(熔点:﹣76℃,沸点:138℃),且易与水发生水解反应,可能生成H2S、SO2、H2SO3、H2SO4等物质.它是橡胶硫化剂.在熔融的硫中通以氯气即可生成S2Cl2 . 下图是实验室用S和Cl2制备S2Cl2的装置(夹持装置、加热装置均已略去). 
(1)已知S2Cl2分子结构与H2O2相似,则S2Cl2的分子中共含有条共价键.
(2)装置a中应放试剂为;装置d的名称是 , 它的作用是 .
(3)该实验的操作顺序应为(用序号表示). ①加热装置c ②通入Cl2③通冷凝水 ④停止通Cl2⑤停止加热装置c
(4)图中f装置中应放置的试剂为 , 其作用为 .
(5)将S2Cl2的水解气体产物通入氯水中,若观察到的现象,则可证明水解产物中有硫化氢生成.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于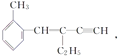 ,下列结论正确的是( )
,下列结论正确的是( )
A. 该有机物分子式为C13H16 B. 该有机物属于苯的同系物
C. 该有机物分子至少有4个碳原子共直线 D. 该有机物分子最多有13个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物检验方法正确的是( )
A.取少量卤代烃加NaOH水溶液共热,冷却,再加AgNO3溶液检验卤原子存在
B.苯和乙烯都能使溴水褪色,但褪色的原理是不同的
C.用溴水可以鉴别乙烯与乙炔
D.苯和苯的同系物都可以用酸性高锰酸钾溶液鉴别
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com