
| ��Ӧǰ�����ʵ����ʵ���/mol | |||
| A | B | C | |
| �� | 6 | 2 | 0 |
| �� | 0 | 0 | 6 |
| �� | 6 | 2 | 6 |
| A�� | ����ƽ��ʱ������A���ܶ��Ǽ��е�2�� | |
| B�� | ����Ӧ��ʼʱ�������м���AΪ2mol��BΪ0.5mol��CΪ3mol����Ӧv��������v���棩 | |
| C�� | ����ƽ��ʱ������A��ת���ʵ�������C��ת���� | |
| D�� | �����ֺ��º�ѹ���ﵽƽ����������������ٳ���2molC��C�İٷֺ������� |
���� ���ݻ�ѧƽ��Ľ���������ʽ��ʽ���㣬
�������� 3A��g��+B��g��?3C��g��
��ʼ����mol�� 6 2 0
�仯����mol�� 3.6 1.2 3.6
ƽ������mol�� 2.4 0.8 3.6
�������кͼ������ﵽ��ͬƽ��״̬
3A��g��+B��g��?3C��g��
��ʼ����mol�� 0 0 6
�仯����mol�� 2.4 0.8 2.4
ƽ������mol�� 2.4 0.8 3.6
���������б��дﵽ��ƽ��
3A��g��+B��g��?3C��g��
6 2 6
��ʼ����mol�� 12 4 0
�൱�ڼ�������2��������Ӧǰ�������С��ѹǿ����ƽ��������У�
��� �⣺���ݻ�ѧƽ��Ľ���������ʽ��ʽ���㣬
�������� 3A��g��+B��g��?3C��g��
��ʼ����mol�� 6 2 0
�仯����mol�� 3.6 1.2 3.6
ƽ������mol�� 2.4 0.8 3.6
�������кͼ������ﵽ��ͬƽ��״̬
3A��g��+B��g��?3C��g��
��ʼ����mol�� 0 0 6
�仯����mol�� 2.4 0.8 2.4
ƽ������mol�� 2.4 0.8 3.6
���������б��дﵽ��ƽ��
3A��g��+B��g��?3C��g��
6 2 6
��ʼ����mol�� 12 4 0
�൱�ڼ�������2��������Ӧǰ�������С��ѹǿ����ƽ��������У�
A���������е���ʼ�����ڼ�������2��������Ӧǰ�������С��ѹǿ����ƽ��������У������A��Ũ�ȱȼ������е�2��С����A����
B���Լ�Ϊ����ƽ�ⳣ��K=$\frac{3��{6}^{3}}{2��{4}^{3}��0.8}$=4.2������AΪ2mol��BΪ0.5mol��CΪ3mol��Ũ����QC=$\frac{{3}^{3}}{{2}^{3}��0.5}$=6.75��K���������ƶ���v��������v���棩����B����
C�����������������ﵽ��ͬ��ƽ��״̬����Ϊ��Чƽ�⣬ƽ��ʱ����A��ת����+����C��ת����=1�����߲��ȣ���C����
D�����ֺ��º�ѹ���ﵽƽ����������������ٳ���2molC�������������������ϵ�������������ֳ������ﵽ��Чƽ�⣬ƽ��ʱ����ְٷֺ�����ȣ���D��ȷ��
��ѡD��
���� ���⿼���˻�ѧƽ�������ʽ����Ӧ�ã���Чƽ��ķ����ж��ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������=A-n | B�� | ������=A-Z | C�� | ������=Z+n | D�� | ���������=n |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
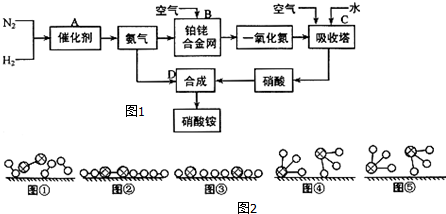
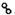 ��
�� ��
��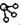 �ֱ��ʾH2��N2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں͢ۺ���ֱ���N2��H2�������ڴ������桢�ڴ������棬N2��H2�л�ѧ�����ѣ�
�ֱ��ʾH2��N2��NH3��ͼ�ݱ�ʾ���ɵ�NH3�뿪�������棬ͼ�ں͢ۺ���ֱ���N2��H2�������ڴ������桢�ڴ������棬N2��H2�л�ѧ�����ѣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
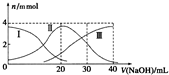 �����£���20mlH2A��Һ�еμ���ͬ���ʵ���Ũ��NaOH��Һ���й������ʵ����仯��ͼ��ʾ�����Т����H2A�������HA-�������A2-��������˵����ȷ���ǣ�������
�����£���20mlH2A��Һ�еμ���ͬ���ʵ���Ũ��NaOH��Һ���й������ʵ����仯��ͼ��ʾ�����Т����H2A�������HA-�������A2-��������˵����ȷ���ǣ�������| A�� | H2A��ˮ�е��뷽��ʽΪ��H2A?2H++A2- | |
| B�� | V��NaOH��=20mlʱ����Һ������ | |
| C�� | V��NaOH��=30mLʱ����Һ�������¹�ϵ��c��A2-��+c��H2A��+c��HA-��=c��Na+�� | |
| D�� | V��NaOH��=40mLʱ����Һ�������¹�ϵ��c��H+��+c��HA-��+c��H2A��=c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ̼ | �� | Y | |
| X | �� | Z |
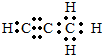 ��Q��ˮ��Ӧ�Ļ�ѧ����ʽΪMg2C3+4H2O=2Mg��OH��2+C3H4����
��Q��ˮ��Ӧ�Ļ�ѧ����ʽΪMg2C3+4H2O=2Mg��OH��2+C3H4�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
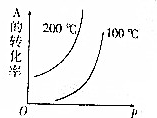 ���ڿ��淴Ӧ��mA��g��+nB��g��?pC��g��+qD��g����m��n��p��q��Ϊ��ѧ��������������ͼʾ���ش�
���ڿ��淴Ӧ��mA��g��+nB��g��?pC��g��+qD��g����m��n��p��q��Ϊ��ѧ��������������ͼʾ���ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2��10-3 | B�� | 2��10-2 | C�� | 2��10-1 | D�� | 2��10-4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 106g | B�� | 90.7g | C�� | 77.8g | D�� | 66.9g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
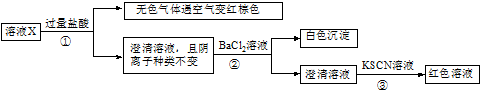
| A�� | ��ɫ���������NO��CO2�Ļ���� | |
| B�� | ԭ��Һ���ܴ���Fe3+ | |
| C�� | ��ҺX���������������4�� | |
| D�� | ��ȡl00mLԭ��ҺX������������NaOH��Һ����ַ�Ӧ����ˣ�ϴ�ӣ����������أ������ϵõ��Ĺ�������Ϊ2.4g |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com