
以下四种金属中属于有色金属的是( )
A.铁 B.铬
C.锰 D.铜
科目:高中化学 来源: 题型:
向明矾[KAl(SO4)2·12H2O]溶液中滴加Ba(OH)2溶液,当SO42-恰好完全沉淀时,铝元素的存在形式为 ( )
A.Al(OH)3、Al3+ B.Al(OH)3 C.Al(OH)3、AlO2— D.AlO2—
查看答案和解析>>
科目:高中化学 来源: 题型:
某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
 (1)A的分子式为 :
(1)A的分子式为 :
 (2)A与溴的四氯化碳溶液反应的化学方程式为 ,反应类型是 ;
(2)A与溴的四氯化碳溶液反应的化学方程式为 ,反应类型是 ;
 (3)已知:
(3)已知: 。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式 ;
。请写出A与稀、冷的KMnO4溶液在碱性条件下反应的化学方程式 ;
 (4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式 ;
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式 ;
 (5)在一定条件下,由A聚合得到的高分子化合物的结构简式为 。
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是( )
A.Al B.Al(OH)3
C.AlCl3 D.Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.铁的应用经历了“铁—普通钢—不锈钢等特种钢”的演变过程
B.减少生铁里的碳元素,并增加硅、锰等元素,即转化为钢
C.普通钢中的含铬量一般在12%以上
D.不锈钢是在普通钢的基础上,加入铬、镍等多种元素炼成的钢材
查看答案和解析>>
科目:高中化学 来源: 题型:
1)已知Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下(所取溶液体积均为10 mL):
| 实验编号 | 实验温度/℃ | c(Na2S2O3) /mol·L-1 | c(H2SO4) /mol·L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
其他条件不变时,探究温度对化学反应速率的影响,应选择__________(填实验编号);探究浓度对化学反应速率的影响,应选择__________(填实验编号);若同时选择①②③溶液变浑浊的同时,探究__________对化学反应速率的影响。
(2)已知Na2S2O3溶液与Cl2反应时,1 mol Na2S2O3转移8 mol电子。该反应的离子方程式是____________________________________________________________,
甲同学设计如下实验流程探究Na2S2O 3的化学性质。
3的化学性质。
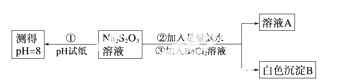
(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和________性。
(Ⅱ)加入BaCl2溶液生成白色沉淀B的离子方程式是________________________。
(Ⅲ)乙同学认为应将上述流程中②③所加试剂顺序颠倒,你认为甲、乙两同学的设计更合理的是________(填“甲”或“乙”),理由是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2=6SO2+Fe3O4,氧化产物为 ,若有3mol FeS2参加反应,转移 mol电子。
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为 (用离子方程式表示)。
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为 。
(4)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有无色气体逸出,请写出相应的离子方程式: 。
(5)铁红是一种红色颜料,其成分是Fe2O3将一定量的铁红溶于160mL 5mol•L-1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),往反应后溶液中滴加KSCN溶液,无明显现象,则参加反应的铁粉的质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应2H2S(g)  2H2(g)+S2(g) ΔH >0,其他条件不变,下列说法正确的是
2H2(g)+S2(g) ΔH >0,其他条件不变,下列说法正确的是
A.加入催化剂,反应路径将发生改变,ΔH也将随之改变
B.升高温度,正逆反应速率都增大,H2S分解率也增大
C.增大压强,平衡向逆反应方向移动,体系温度降低
D.恒容体系,充入H2重新达到平衡后,H2浓度将减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com