
【题目】下表给出了五种元素的相关信息,其中A、B、C、D为短周期元素.
元素 | 相关信息 |
A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为倍受青睐的清洁燃料. |
B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障. |
C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂. |
D | 室温下其单质呈粉末固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰. |
E | 它是人体不可缺少的微量元素,其单质也是工业生产中不可缺少的金属原材料,常用于制造桥梁、轨道等. |
(1)E在元素周期表中的位置是 .
(2)B和D对应的气态氢化物中,稳定性强的是 , 熔沸点高的是(用具体的化学式表示).
(3)D的单质与烧碱水溶液加热时发生自身氧化还原反应生成两种具有强还原性的阴离子,写出该反应的离子方程式 .
(4)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1:2)一起用作火箭助推剂,写出两者发生反应生成无毒物质的化学方程式 .
(5)以上这五种元素组成一种工业上用途极广的复盐,该物质中A、B、C、D、E的质量比为5:56:7:16:14.则其水溶液的pH7(填“>”“=”或“<”),原因是(用离子方程式表示).溶液中离子浓度从大到小的顺序为 .
【答案】
(1)第四周期第Ⅷ族
(2)H2O;H2O
(3)3S+6OH﹣ ![]() SO
SO ![]() +2S2﹣+3H2O
+2S2﹣+3H2O
(4)2N2H4+N2O4 ![]() 3N2+4H2O
3N2+4H2O
(5)<;Fe2++2H2O?Fe(OH)2+2H+、NH4++H2O?NH3?H2O+H+;c(NH4+)>c(SO ![]() )>c(Fe2+)>c(H+)>c (OH﹣)
)>c(Fe2+)>c(H+)>c (OH﹣)
【解析】解:由题目信息可知,A为H,B为O,C为N,D为S,E为Fe.(1)Fe位于第四周期第Ⅷ族,所以答案是:第四周期第Ⅷ族;(2)非金属性O>S,故H2O和H2S中,H2O稳定性较强,H2O由于存在分子间氢键,所以熔沸点较H2S高,所以答案是:H2O;H2O;(3)S与NaOH溶液该反应生成亚硫酸钠、硫化钠与水,反应离子方程式为:3S+6OH﹣ ![]() SO32﹣+2S2﹣+3H2O,所以答案是:3S+6OH﹣
SO32﹣+2S2﹣+3H2O,所以答案是:3S+6OH﹣ ![]() SO32﹣+2S2﹣+3H2O;(4)C与A形成的原子个数比为1:2的化合物为N2H4 , C与B形成的原子个数比为1:2的化合物为N2O4 , N2H4与N2O4反应生成氮气与水,反应方程式为:2N2H4+N2O4
SO32﹣+2S2﹣+3H2O;(4)C与A形成的原子个数比为1:2的化合物为N2H4 , C与B形成的原子个数比为1:2的化合物为N2O4 , N2H4与N2O4反应生成氮气与水,反应方程式为:2N2H4+N2O4 ![]() 3N2+4H2O,所以答案是:2N2H4+N2O4
3N2+4H2O,所以答案是:2N2H4+N2O4 ![]() 3N2+4H2O;(5)根据质量比可得H、O、N、S、Ee元素原子个数比为
3N2+4H2O;(5)根据质量比可得H、O、N、S、Ee元素原子个数比为 ![]() :
: ![]() :
: ![]() :
: ![]() :
: ![]() =20:14:2:2:1,故此盐为(NH4)2SO4FeSO46H2O,溶液中Fe2+与NH4+均水解:Fe2++2H2OFe(OH)2+2H+、NH4++H2ONH3H2O+H+ , 故溶液显酸性,溶液中各离子浓度由大到小排列为:c(NH4+)>c(SO
=20:14:2:2:1,故此盐为(NH4)2SO4FeSO46H2O,溶液中Fe2+与NH4+均水解:Fe2++2H2OFe(OH)2+2H+、NH4++H2ONH3H2O+H+ , 故溶液显酸性,溶液中各离子浓度由大到小排列为:c(NH4+)>c(SO ![]() )>c(Fe2+)>c(H+)>c (OH﹣),所以答案是:<;Fe2++2H2OFe(OH)2+2H+、NH4++H2ONH3H2O+H+;c(NH
)>c(Fe2+)>c(H+)>c (OH﹣),所以答案是:<;Fe2++2H2OFe(OH)2+2H+、NH4++H2ONH3H2O+H+;c(NH ![]() )>c(SO
)>c(SO ![]() )>c(Fe2+)>c(H+)>c (OH﹣).
)>c(Fe2+)>c(H+)>c (OH﹣).


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】在25℃,101kPa条件下,将15L O2通入10LCO和H2的混合气中,使其完全燃烧,干燥后,恢复至原来的温度和压强.
(1)若剩余气体的体积是15L,则原CO和H2的混合气中V(CO)=L,V(H2)=L.
(2)若剩余气体的体积为a L,则原CO和H2的混合气中V(CO):V(H2)= .
(3)若剩余气体的体积为aL,则a的取值范围是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于A2+3B2 ![]() 2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
2C的反应来说,以下化学反应速率的表示中,反应速率最快的是( )
A.v(B2)=0.8mol/(Ls)
B.v(A2)=0.4mol/(Ls)
C.v(C)=0.6mol/(Ls)
D.v(B2)=4.2mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关用惰性电极电解AgNO3溶液的说法不正确的是( )
A.电解过程中阴极质量不断增大
B.电解过程中阳极附近的pH不断降低
C.电解一段时间后,向溶液中加入适量的Ag2O固体可使溶液恢复到电解前的状况
D.电解过程中,溶液中电子由阴极迁向阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列离子方程式对应的一个化学方程式:
(1)2H+ + CO32— = H2O + CO2↑ (2) 2OH-+ Cu2+ = Cu(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向密闭容器中充入1mol NO和1mol CO进行反应:NO(g)+CO(g) ![]() N2(g)+CO2(g),测得化学反应速率随时间的变化关系如图所示,其中处于化学平衡状态的点是( )
N2(g)+CO2(g),测得化学反应速率随时间的变化关系如图所示,其中处于化学平衡状态的点是( ) 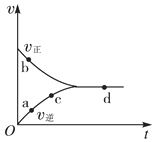
A.a点
B.b点
C.c点
D.d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是
A. 做“氢气还原氧化铜”实验时,应先通氢气再加热
B. 蒸馏时烧瓶中一般要放入碎瓷片防止暴沸
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应该先关冷凝水再撤酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的氧气和Y气体,在相同温度、相同容积的密闭容器中,氧气的压强大于Y气体,则Y可能为( )
A. CH4B. NOC. C2H4D. CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有如下三个热化学方程式:
H2(g)+ ![]() O2(g)═H2O(g)△H=a kJmol﹣1
O2(g)═H2O(g)△H=a kJmol﹣1
H2(g)+ ![]() O2(g)═H2O(l)△H=b kJmol﹣1
O2(g)═H2O(l)△H=b kJmol﹣1
2H2(g)+O2(g)═2H2O(l)△H=c kJmol﹣1
关于它们的下列表述正确的是( )
A.它们都是吸热反应
B.a、b和c均为正值
C.a=b
D.2b=c
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com