
ij»ÆѧŠĖȤŠ”×éÓū²ā¶ØÄ³Ę·ÅĘĪ¶¾«ÖŠĀČ»ÆÄʵÄŗ¬Į攣øĆŠ”×éµÄŹµŃé²½ÖčČēĻĀ£ŗ
¢Ł³ĘČ”øĆĪ¶¾«ŃłĘ·10.0g·ÅČėÉÕ±ÖŠ£¬²¢¼ÓŹŹĮæÕōĮóĖ®ĶźČ«Čܽā£»
¢Ś¼ÓČė¹żĮæµÄÓĆĻõĖįĖį»ÆµÄĻõĖįŅųČÜŅŗ£Ø¼Ł¶ØÖ»ÓŠNaClÓėAgNO3ČÜŅŗ·“Ó¦£©”£
¢Ū¹żĀĖ£»
¢ÜÓĆÕōĮóĖ®Ļ“µÓ³Įµķ2”«3“Ī£»
¢Ż½«³ĮµķŗęøÉ”¢³ĘĮ棬²āµĆĘäÖŹĮæĪŖ5.74g£»
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ÉĻŹöŹµŃé²½Öč¢Ū²Ł×÷ÖŠĖłÓƵ½µÄ²£Į§ŅĒĘ÷ÓŠ ”£
£Ø2£©Čō“ĖĘ·ÅĘĪ¶¾«°ü×°“üÉĻ±ź×¢£ŗ”°¹Č°±ĖįÄĘŗ¬Įæ”Ż80.0% ,ĀČ»ÆÄĘŗ¬Įæ”Ü20.0%”±£»£Ø¼ŁÉčѳʷ֊²»ŗ¬ĘäĖüŌÓÖŹ£©”£ĶعżÉĻŹöŹµŃé½į¹ū£¬æɼĘĖć³öѳʷ֊ĀČ»ÆÄʵÄÖŹĮæ·ÖŹżĪŖ £¬ĖłŅŌøĆѳʷ £ØĢī”°ŗĻøń”±»ņ”°²»ŗĻøń”±£©”£
£Ø3£©¼ģŃéÉĻŹöŹµŃé²½Öč¢ÜĖłµĆ³ĮµķŹĒ·ńĻ“¾»µÄ·½·ØŹĒ£ŗČ”×īŗóŅ»“ĪĻ“µÓŅŗÉŁĮ棬
ӣ
”¾“š°ø”æ39”¢£Ø1£©Ā©¶·”¢²£Į§°ō”¢ÉÕ± £Ø2£©23.4% ²»ŗĻøń £Ø3£©µĪ¼ÓĻ”ŃĪĖį£¬¹Ū²ģÓŠĪŽ³Įµķ²śÉś”£
”¾½āĪö”æ£Ø1£©ŌŚ½ųŠŠ¹żĀĖ²Ł×÷Ź±£¬³żĮĖŹ¹ÓĆĢś¼ÜĢØĶā£¬»¹ŅŖÓƵ½Ā©¶·”¢²£Į§°ō”¢ÉÕ±µČ²£Į§ŅĒĘ÷£¬£Ø2£©µĪČėĻõĖįŅųŹĒĪŖĮĖ½«ĀČ»ÆÄĘÖŠµÄĀČ×Ŗ»ÆĪŖæɳĮµķµÄĀČ»ÆŅų£¬¼ÓČėĻ”ĻõĖįµÄÄæµÄŹĒ½«ĘäĖüŌÓÖŹ²śÉśµÄ³ĮµķČܽā³żČ„£»Éčѳʷ֊ĀČ»ÆÄʵÄÖŹĮæĪŖx£¬Ōņøł¾Ż·½³ĢŹ½ÓŠ£ŗ
NaCl+AgNO3 =AgCl”ż+NaNO3
58.5 143.5
x 5.74 x=£Ø58.5”Į5.74£©/143.5= 2.34g
ĖłŅŌѳʷ֊ĀČ»ÆÄʵÄŗ¬ĮæĪŖ£ŗ2.34/10”Į100%=23.4%
¶ų23.4%£¾20%£¬“Ėѳʷ²»·ūŗĻ²śĘ·±źŹ¾µÄÖŹĮæ·ÖŹż.
(3) ¼ģŃéÉĻŹöŹµŃé²½Öč¢ÜĖłµĆ³ĮµķŹĒ·ńĻ“¾»µÄ·½·ØŹĒ£ŗČ”×īŗóŅ»“ĪĻ“µÓŅŗÉŁĮæµĪ¼ÓĻ”ŃĪĖį£¬¹Ū²ģÓŠĪŽ³Įµķ²śÉś.


 ѧĮ·æģ³µµĄæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
ѧĮ·æģ³µµĄæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪŖ²ā¶ØĘųĒņÄŚµÄĘųĢå³É·Ö£¬ÓŠµÄѧɜÓĆ³¬±”µÄĘųĒņ°“ČēĶ¼×°ÖĆ½ųŠŠŹµŃ锣æŖŹ¼Ź±ĘųĒņ³ĮÓŚÉÕ±µ×²æ£¬“ņæŖæŖ¹Ųŗ󣬹żŅ»»į¶łĘųĒņ“ÓÉÕ±µ×²æĀżĀżø”Ęš£¬×īŗóŠüÓŚÉÕ±æŚ”£ĘųĒņÄŚŹ¢·ÅµÄĘųĢåæÉÄÜŹĒ(””””)xk|b|1
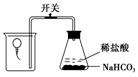
A£®O2 B£®H2
C£®NH3 D£®SO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓƵ¼Ļß½«ĶʬŗĶŠæʬĮ¬½Óŗó²åČėĻ”ĮņĖįÖŠ×é³ÉŌµē³Ų£¬ĘäÖŠĶʬ×÷
A£®Ńō¼« B£®Ņõ¼« C£®Õż¼« D£®øŗ¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŅ»¶ØĪĀ¶ČĻĀµÄĆܱÕČŻĘ÷ÖŠ, ŅŃ“ļĘ½ŗāדĢ¬µÄĻĀĮŠ·“Ó¦£ŗA(s)+2B(g)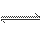 C(g)+D(g)£¬ ĘäĖüĢõ¼ž²»±äŹ±£¬øıäĻĀĮŠĢõ¼ž£¬Ę½ŗā»į·¢ÉśŅĘ¶ÆµÄŹĒ
C(g)+D(g)£¬ ĘäĖüĢõ¼ž²»±äŹ±£¬øıäĻĀĮŠĢõ¼ž£¬Ę½ŗā»į·¢ÉśŅĘ¶ÆµÄŹĒ
A.¼ÓČČ B. Ōö“óŃ¹Ēæ
C.¼ÓČė“߻ƼĮ D.¼õÉŁCµÄĪļÖŹµÄĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪüŹ³»ņ×¢Éä¶¾Ę·»įĪ£¼°ČĖĢ彔浣¬ĻĀĮŠø÷×éÖŠµÄĪļÖŹ¶¼ŹōÓŚ¶¾Ę·µÄŹĒ
A£®±ł¶¾”¢ĒąĆ¹ĖŲ B£®ŗ£ĀåŅņ”¢±ł¶¾
C£®Äį¹Å¶””¢µāŃĪ D£®“óĀ锢Ņ”Ķ·Ķč
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĪļÖŹµÄĖ×³Ę”¢Ö÷ŅŖ³É·ÖµÄ»ÆѧŹ½¼°ĘäÓĆĶ¾¾łÕżČ·µÄŹĒ
A£®“ÅĢśæó”Ŗ”ŖFe2O3”Ŗ”ŖĮ¶Ģś B£®µØ·Æ”Ŗ”ŖCuSO4”¤5H2O”Ŗ”Ŗ²Ø¶ū¶ąŅŗ
C£®Ą¶±¦ŹÆ”Ŗ”ŖSiO2”Ŗ”ŖŹĪĘ· D£®“æ¼ī”Ŗ”ŖNaHCO3”Ŗ”Ŗ±ŗÖĘøāµć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®³£ĪĀ”¢³£Ń¹ĻĀ£¬16 g O3ÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖNA
B£®7.8 g Na2O2ÓėĖ®³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.2 NA
C£®0.1 mol FeÓė0.1 mol Cl2³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.3NA
D£®±ź×¼×“æöĻĀ£¬11.2 L H2OÖŠŗ¬ÓŠµÄĒāŌ×ÓŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ČōNA±ķŹ¾°¢·š¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ( )
A£®1 mol Cl2×÷ĪŖŃõ»Æ¼ĮµĆµ½µÄµē×ÓŹżĪŖNA
B£®ŌŚ0 ”ę£¬101 kPaŹ±£¬22.4 LĒāĘųÖŠŗ¬ÓŠNAøöĒāŌ×Ó
C£®14 gµŖĘųÖŠŗ¬ÓŠ7 NAøöµē×Ó
D£®NAøöŅ»Ńõ»ÆĢ¼·Ö×ÓŗĶ0.5 molCH4Ėłŗ¬Ō×ÓŹżĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬½«ĘųĢåXŗĶĘųĢåYø÷0.16 mol³äČė10 LŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦X(g)£«Y(g)  2Z(g)””¦¤H£¼0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČēĻĀ±ķ£ŗ
2Z(g)””¦¤H£¼0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČēĻĀ±ķ£ŗ
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A£®·“Ó¦Ē°2 minµÄĘ½¾łĖŁĀŹv(Z)£½2.0”Į10£3 mol/(L·min)
B£®ĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Č£¬·“Ó¦“ļµ½ŠĀĘ½ŗāĒ°vÄę£¾vÕż
C£®øĆĪĀ¶ČĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK£½1.44
D£®ĘäĖūĢõ¼ž²»±ä£¬ŌŁ³äČė0.2 mol Z£¬Ę½ŗāŹ±XµÄĢå»ż·ÖŹżŌö“ó
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com