
(本小题14分)下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
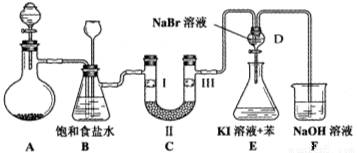
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:________________________。
(2)装置B中饱和食盐水的作用是________________________________________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象______________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入__________。
| A | B | C | D |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E的目的是 。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_______________________________。
(5)某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,老师认为不妥,用总反应的离子方程式解释原因_____________________________________。
17.(本小题14分,每空2分)(1)Ca(ClO)2+4HCl(浓)==CaCl2+2Cl2↑+2H2O
(2)除去Cl2中HCl ;B中长颈漏斗内液面上升,形成一段水柱,锥形瓶内液面下降;(3)D
(4)比较氯、溴、碘的非金属性强弱 E中溶液分为两层,上层液体为紫红色
(5)4HSO3-+Cl2=SO42-+2Cl-+3SO2+2H2O。
【解析】
试题分析:(1)漂粉精固体的有效成分是Ca(ClO)2,它和浓盐酸反应的化学反应方程式为Ca(ClO)2+4HCl(浓)==CaCl2+2Cl2↑+2H2O;(2)由于浓盐酸有挥发性,所以在制取的Cl2中含有HCl杂质,装置B中饱和食盐水的作用是除去Cl2中HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗内液面上升,形成一段水柱,锥形瓶内液面下降;(3)装置C的实验目的是验证氯气是否具有漂白性,所以Ⅰ中湿润的有色布条,看到褪色;由于是在U型管,所以应该是固体干燥剂,而浓硫酸是液体,不能使用,所以Ⅱ中放无水氯化钙来吸收水,Ⅲ中放干燥的有色布条不褪色,证明有漂白作用的是HClO,而不是Cl2。选项是D。(4)设计装置D、E的目的是比较氯、溴、碘的非金属性强弱。打开活塞,将装置D中少量溶液加入装置E中,振荡。由于Cl2会与NaBr、KI发生氧化还原反应产生Br2、I2, I2容易溶解在苯中,苯与水互不相溶,I2溶解在苯中得到的溶液是紫色,因此会观察到的现象是E中溶液分为两层,上层液体为紫红色;(5)氯气能够与NaOH发生反应产生无毒的物质,但是某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,但是老师认为不妥,原因是氯气与水发生反应产生的HClO把NaHSO3氧化为SO42-。还会发生产生的盐酸会与NaHSO3发生反应产生SO2,用总反应的离子方程式解释是4HSO3-+Cl2=SO42-+2Cl-+3SO2+2H2O。
考点:考查氯气的制取、性质验证、实验现象、操作方法及两种方程式的书写的知识。


科目:高中化学 来源:2015届北京市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列事实与胶体性质无关的是
A.可用半透膜除去淀粉溶液中的少量NaCl
B.黄河入海口容易形成沙洲
C.将植物油倒入水中用力搅拌可形成油水混合物
D.一束平行光线通过蛋白质溶液,从侧面可以看到一条光亮的通路
查看答案和解析>>
科目:高中化学 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
下列选项中的原因或结论与现象不对应的是
选项 | 现象 | 原因或结论 |
A | 在 H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
B | 向5mL 0.005mol·L-1FeCl3溶液中加入5mL 0.015mol·L-1KSCN溶液,溶液呈红色,再滴加几滴1mol·L-1KSCN溶液,溶液颜色加深 | 增大反应物浓度,平衡向正反应方向移动 |
C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 该反应△H<0,平衡向生成NO2方向移动 |
D | 在密闭容器中有反应:A+xB(g) | A非气体、x=1 |
查看答案和解析>>
科目:高中化学 来源:2015届北京市朝阳区高三年级第一学期期中统一考试化学试卷(解析版) 题型:选择题
重水(2H2O)是重要的核工业原料,下列说法不正确的是
A.氘( )原子核内有1个质子
)原子核内有1个质子
B.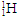 与
与 是不同的核素
是不同的核素
C.1H2O与2H2O是同一种物质
D.1H218O与2H216O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源:2015届北京市东城区普通校高三11月联考化学试卷(解析版) 题型:选择题
氮化铝广泛应用于电子、陶瓷等工业领域。在一定条件下,AlN可通过反应Al2O3+N2+3C =2AlN+3CO合成。下列叙述正确的是
A.上述反应中,N2是还原剂,Al2O3是氧化剂
B.上述反应中,每生成1 mol AlN需转移3 mol电子
C.AlN中氮元素的化合价为+3
D.AlN的摩尔质量为41 g
查看答案和解析>>
科目:高中化学 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
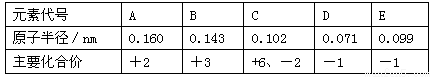
A.A、B的单质与稀盐酸反应速率B>A
B.D、E形成的简单离子的还原性E->D-
C.气态氢化物的稳定性HD<H2C
D.最高价氧化物对应的水化物的酸性 H2CO4>HEO4
查看答案和解析>>
科目:高中化学 来源:2015届北京十中高三第一学期期中化学试卷(解析版) 题型:选择题
若NA表示阿伏加德罗常数,下列说法正确的是
A.标准状况下,6.72LNO2与水充分反应转移电子数为0.1NA
B.18gD2O中含有的质子数目为10NA
C.常温常压下,1mol氦气中含有的核外电子数为2NA
D.ag某气体含分子数为b,cg该气体在标况下的体积为22.4ab/(c NA) L。
查看答案和解析>>
科目:高中化学 来源:2015届内蒙古赤峰市高三上学期9月质量检测化学试卷(解析版) 题型:选择题
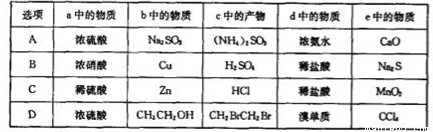
实验室某些物质的制备装置如图所示(省略夹持装置和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的是
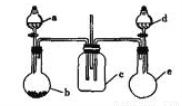
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com