
����Ŀ����֪��298Kʱ��N2(g)+3H2(g)![]() 2NH3(g) ��H=-92.2kJ��mol-1��
2NH3(g) ��H=-92.2kJ��mol-1��
(1)��N��N�ļ���Ϊ941.3kJ��mol-1��H��H�ļ���Ϊ436.4kJ��mol-1����N��H�ļ���Ϊ___��
(2)ʵ���ҽ�1.1molN2��3molH2����2L������һ�������·�Ӧ�������¶Ⱥ�����������䣬
����2minĩ���H2�����ʵ���Ϊ1.8mol�����ʱ�����������ƽ����Ӧ����Ϊ___��
�ڱ����¶Ⱥ�����������䣬���д�ʩ�ɼӿ�÷�Ӧ���ʵ���___��
A.����He��
B.ʹ��ǡ���Ĵ���
C.���߷�Ӧ��ϵ���¶�
D.�ٳ���N2
�۵��������������ֲ���ʱ�������÷�Ӧһ�����ڻ�ѧƽ��״̬����___��
A.������N2��H2���
B.�����������ܶ�
C.������������ѹǿ
D.H2�����ʵ���
(3)�绯ѧ���������������ڼ�����NH3�ĺ������乤��ԭ����ͼ��ʾ��
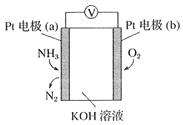
�����·�������˶�����___��(����a����b��������b����a����)��
��b���缫��ӦʽΪ___��
���𰸡�390.5kJmol-1 0.2mol/(Lmin) BCD ACD b����a�� O2+4e��+2H2O=4OH��
��������
(1)![]() =��Ӧ�����֮��-���������֮�ͣ���N��H������Ϊx������941.3kJmol-1+3��436.4kJmol-1-x��6=-92.2kJmol-1�����x=390.5kJmol-1��
=��Ӧ�����֮��-���������֮�ͣ���N��H������Ϊx������941.3kJmol-1+3��436.4kJmol-1-x��6=-92.2kJmol-1�����x=390.5kJmol-1��
(2)��2min�ڲμӷ�ӦH2�����ʵ���Ϊ3mol-1.8mol=1.2mol���������ķ�Ӧ����Ϊ![]() =0.3mol/(Lmin)���ɷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�������ƽ����Ӧ����Ϊ0.3mol/(Lmin)��
=0.3mol/(Lmin)���ɷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ�������ƽ����Ӧ����Ϊ0.3mol/(Lmin)��![]() =0.2mol/(Lmin)��
=0.2mol/(Lmin)��
��A������He������������䣬��Ӧ�и����ʵ�Ũ�Ȳ��䣬��Ӧ���ʲ��䣬��A��ѡ��
B��ʹ��ǡ���Ĵ����������˷�Ӧ����Ļ�ܣ���Ӧ���ʼӿ죬��Bѡ��
C�����߷�Ӧ��ϵ���¶ȣ�����ӵİٷ�������Ӧ���ʼӿ죬��Cѡ��
D���ٳ���N2����Ӧ���Ũ�ȱ��Ӧ���ʼӿ죬��Dѡ��
�ʴ�Ϊ��B��C��D��
��A��������N2��H2�ĺ�������ʱ��˵�����淴Ӧ������ȣ���ѧ��Ӧ�ﵽƽ�⣬��Aѡ��
B����Ӧ������ɾ�Ϊ���壬������������ʼ�ղ��䣬�������ݣ����������������ܶ�ʼ�ղ��䣬�������������ܶȲ��䲻���жϻ�ѧ��Ӧ�ﵽƽ�⣬��B��ѡ��
C���÷�Ӧǰ������ϵ��֮�Ͳ���ȣ�δƽ��ʱ����������ʵ�����䣬�������ݣ�����ѹǿ��䣬��ѹǿ����ʱ��˵����Ӧƽ�⣬��Cѡ��
D��H2�����ʵ������䣬��Ũ�Ȳ��䣬���淴Ӧ������ȣ���ѧ��Ӧ�ﵽƽ�⣬��Dѡ��
�ʴ�Ϊ��A��C��D��
(3)�پ�ͼ��֪�ŵ������NH3ת��ΪN2�����������Ե缫aΪ�������缫bΪ������ԭ��������·������������������b����a����
��b���������õ��ӷ�����ԭ��Ӧ���������Һ�Լ��ԣ�����b���缫����ʽΪ��O2+4e��+2H2O=4OH����


 ��У��������ĩ��̾�ϵ�д�
��У��������ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��M��N��X��Y��Z��ԭ��������������������ɵĵ��ʻ����������ת����ϵ���ס���Ϊ��Ԫ������(����Ԫ���γɵĻ�������ҡ���Ϊ���ʣ�������Ϊ��Ԫ�������֪25��ʱ��0.1mol/L�ļס�������Һ��pH�ֱ�Ϊl��13 ������������Һ���ʱ������ɫ�����������ƶ���ȷ����

A. M�ֱ���N��X��Z�γɵļ������У�M��N�γɵĻ������۵����
B. ԭ�Ӱ뾶��Z>Y>X>M>N
C. X��Y��Z������������Ӧ��ˮ���������Ӧ
D. Z�������ӽ�����ӵ�������N��������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ���ǣ� ��
A.�������Һ�еμ�Ũ��ˮ��������CH3COOH+OH-=CH3COO-+H2O
B.���Ȼ�����ʴӡˢ��·�壺Fe3++Cu=Fe2++Cu2+
C.����������ϡ���ᷴӦ��FeO+2H+=Fe2++H2O
D.����̼�������Һ�������ռ���Һ��ϼ��ȣ�NH![]() +HCO
+HCO![]() +2OH-
+2OH-![]() NH3��+CO
NH3��+CO![]() +2H2O
+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǵؿ��к������Ľ���Ԫ�أ�����Ȼ����Ҫ�Ի���̬����ʽ�������������С����������Ҫ�ɷ���Al2O3�������������SiO2��Fe2O3�����ʣ�ұ������������Ҫ��һ��������Al2O3���ᴿ������Al2O3�����������������SiO2�����������Fe2O3�Ǽ����������ͼΪ��ҵ�������ܷ���ȡ�������е�����

���ۻش��������⣺
(1)���м������ij�����Ҫ��___________(��ѧʽ)��Ϊ�˼ӿ��������������е��ܽ⣬�ɲ�ȡ�Ĵ�ʩ��___________________________��һ�ּ��ɣ���
(2)д���ڡ����п��ܷ�����Ӧ�����ӷ���ʽ��
��_______________________��________________��_______________________��________________��
��_____________________��________________��
(3)������в��ð�ˮ����Fe3����ԭ��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Y���п������������ã�����X�Ƶã�

�����йػ�����X��Y��˵������ȷ����
A.1 mol X�������3 mol NaOH��Ӧ
B.Y������������һ�������·�Ӧ�ɵõ�X
C.X��Y��Ϊͬϵ��
D.������X��Y�ֱ�������Br2�ӳɵIJ������������̼ԭ����Ŀ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������������ȷ����(����)
A. 1 mol����һ�������·ֱ������������������ȫ��Ӧת�Ƶ�������Ϊ2NA
B. 30 g�����Ǻͱ�����Ļ�����к��е���ԭ����Ϊ4NA
C. 12 gʯīϩ(����ʯī)�к�����Ԫ���ĸ���Ϊ2NA
D. 2.1 g DTO�к��е�������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����ת����ϵ��ͼ��ʾ������BΪ����ɫ��C����ʱΪ��ɫҺ������Է�������D��B��17��E��ԭ������Ϊ12��
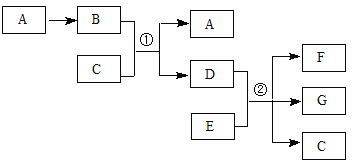
�ش��������⣺
��1��A�Ļ�ѧʽ�� ��C���ӵĵ���ʽ�� ��
��2����Ӧ�������ӷ���ʽ�� ����n��E)��n��D)=2��5����Ӧ�ڵĻ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ��� ����
A. 1 mol H2O���е�������Ϊ10 mol
B. 0.5 mol SO42-��8 mol����
C. 18 gˮ�к��е���ԭ����Ϊ6.02��1022
D. 1 mol NaHSO4�����к��е�������������Ϊ3��6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��5�������о���Ա�ɹ�ʵ���ڳ��³�ѹ���õ�����ˮ��������ԭ������ͼ��ʾ��
����˵����ȷ���ǣ� ��
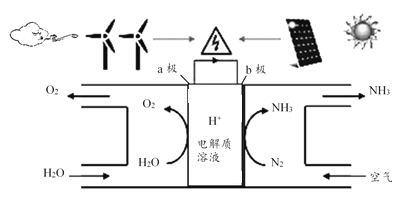
A. ͼ������ת����ʽֻ��2��
B. H+��a�����ƶ�
C. b�������ĵ缫��ӦΪ��N2+6H++6e��=2NH3
D. a����ÿ����22.4LO2�����缫�ĵ�����һ��Ϊ4��6.02��1023
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com