
����Ŀ���������ƣ�NaNO2����һ�ֳ�����ʳƷ���Ӽ���ʹ��ʱ�����ϸ������������ij��ȤС������ͼ��ʾװ���Ʊ�NaNO2����������������̽����A�м���װ������ȥ���� 
��֪����2NO+Na2O2�T2NaNO2��
��NO�ܱ�����KMnO4������NO3�� �� MnO4������ԭΪMn2+ ��
��1���Ʊ�NaNO2
��i��װ��A������ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ ��
��ii��Bװ�õ�Ŀ���� ��
��iii��Ϊ��֤�Ƶõ��������ƵĴ��ȣ�Cװ����ʢ�ŵ��Լ�������������ţ���
A��P2O5 B����ʯ�� C����ˮCaCl2 D����ʯ��
��iv��Eװ�÷�����Ӧ�����ӷ���ʽ�� ��
��2���ⶨNaNO2����
ȷ��ȡ����Ϊm g��NaNO2��Ʒ������ƿ�У�������ˮ�ܽ⣮��a molL��1����KMnO4��Һ�ζ�����ζ��յ�ʱ����KMnO4��Һ���Ϊbml������Ʒ��NaNO2����������Ϊ ��
��������Ʒ����������������KMnO4��Һ����Ӧ���ú�m��a��b�Ĵ���ʽ��ʾ����
���𰸡�
��1��C+4HNO3��Ũ�� ![]() CO2��+4NO2��+2H2O����NO2ת��ΪNO��ͭ��ϡ���ᷴӦ����NO��BD��5NO+3MnO4��+4H+=5NO3��+3 Mn2++2H20
CO2��+4NO2��+2H2O����NO2ת��ΪNO��ͭ��ϡ���ᷴӦ����NO��BD��5NO+3MnO4��+4H+=5NO3��+3 Mn2++2H20
��2��![]()
���������⣺��1����i��װ��A������ƿ�з�����Ӧ�Ļ�ѧ����ʽΪC+4HNO3��Ũ�� ![]() CO2��+4NO2��+2H2O�����Դ��ǣ�C+4HNO3��Ũ��
CO2��+4NO2��+2H2O�����Դ��ǣ�C+4HNO3��Ũ�� ![]() CO2��+4NO2��+2H2O����ii��Bװ�õ�Ŀ���Ǣٽ�NO2ת��ΪNO����ͭ��ϡ���ᷴӦ����NO�����Դ��ǣ���NO2ת��ΪNO��ͭ��ϡ���ᷴӦ����NO����iii��A��C���������ᣬB��D���������Ҹ������壬���Դ��ǣ�BD����iv������Ϣ��֪��Eװ�õ����������ø��������Һ��ǿ���������������ж�����һ�������������ж���NO���壬������Ⱦ��������Ӧ�����ӷ���ʽΪ��5NO+3MnO4��+4H+=5NO3��+3 Mn2++2H20�����Դ��ǣ�5NO+3MnO4��+4H+=5NO3��+3 Mn2++2H20����2����NaNO2�μӵ����Ը��������Һ�У��ɹ۲쵽��ɫ��Һ��ɫ��dz��ֱ����ɫ��˵�����߷���������ԭ��Ӧ������������ӱ�����������������ӣ�����������ӱ���ԭ���������ӣ���NaNO2�μӵ����Ը��������Һ�У��ɹ۲쵽��ɫ��Һ��ɫ��dz��ֱ����ɫ��˵�����߷���������ԭ��Ӧ������������ӱ�����������������ӣ�����������ӱ���ԭ���������ӣ����ӷ���ʽΪ��ȷ��ȡ����Ϊm g��NaNO2��Ʒ������ƿ�У�������ˮ�ܽ⣮��a molL��1����KMnO4��Һ�ζ�����ζ��յ�ʱ����KMnO4��Һ���Ϊbml��
CO2��+4NO2��+2H2O����ii��Bװ�õ�Ŀ���Ǣٽ�NO2ת��ΪNO����ͭ��ϡ���ᷴӦ����NO�����Դ��ǣ���NO2ת��ΪNO��ͭ��ϡ���ᷴӦ����NO����iii��A��C���������ᣬB��D���������Ҹ������壬���Դ��ǣ�BD����iv������Ϣ��֪��Eװ�õ����������ø��������Һ��ǿ���������������ж�����һ�������������ж���NO���壬������Ⱦ��������Ӧ�����ӷ���ʽΪ��5NO+3MnO4��+4H+=5NO3��+3 Mn2++2H20�����Դ��ǣ�5NO+3MnO4��+4H+=5NO3��+3 Mn2++2H20����2����NaNO2�μӵ����Ը��������Һ�У��ɹ۲쵽��ɫ��Һ��ɫ��dz��ֱ����ɫ��˵�����߷���������ԭ��Ӧ������������ӱ�����������������ӣ�����������ӱ���ԭ���������ӣ���NaNO2�μӵ����Ը��������Һ�У��ɹ۲쵽��ɫ��Һ��ɫ��dz��ֱ����ɫ��˵�����߷���������ԭ��Ӧ������������ӱ�����������������ӣ�����������ӱ���ԭ���������ӣ����ӷ���ʽΪ��ȷ��ȡ����Ϊm g��NaNO2��Ʒ������ƿ�У�������ˮ�ܽ⣮��a molL��1����KMnO4��Һ�ζ�����ζ��յ�ʱ����KMnO4��Һ���Ϊbml��
2MnO4��+ | 5NO2��+ | 6H+ | = | 2Mn 2++ | 3H2O+ | 5NO3�� |
2 | 5 | |||||
amol/L��b��10��3L | n |
n= ![]() mol
mol
����Ʒ��NaNO2����������Ϊ ![]() ��100%=
��100%= ![]() ��
��
���Դ��ǣ� ![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������ȷ���� (����)
A. ����ʽ����CnH2n��2����һ��������
B. ������������ˮ����ȡ����Ӧ
C. ��������۷е��������ĸ�
D. �������ܱ����Ը�����ص�ǿ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ�����ܵó��Ľ�����( )
A.H2��O2��Ӧ�Ƿ��ȷ�Ӧ
B.�Ͽ���ѧ��Ҫ�ų�����
C.��ѧ��Ӧ���������ʱ仯�������仯
D.2mol H2��1mol O2�������������2mol H2O ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Dz��ֶ������еڶ�����������Ԫ�ص�ԭ�Ӱ뾶����Ҫ���ϼۡ�
Ԫ�ش��� | �� | �� | �� | �� | �� | �� | �� | �� |
ԭ�Ӱ뾶��nm�� | 0.186 | 0.160 | 0.152 | 0.143 | 0.110 | 0.099 | 0.075 | 0.074 |
��Ҫ���ϼ� | ��1 | ��2 | ��1 | ��3 | ��5����3 | ��7����1 | ��5����3 | ��2 |
�ش��������⣺
��1������Ԫ�����ڱ��е�λ���ǣ����ڡ��壩��
��2��8��Ԫ�ص�����������ˮ�����У�������ǿ�������ѧʽ����
��3��Ԫ�آݡ��ߡ���ֱ��γɵļ���̬�⻯���У��ߵĵ���ʽΪ �� �ȶ�����ǿ���⻯��ĽṹʽΪ��
��4��д���١��ܵ�����������Ӧ��ˮ����֮�䷢����Ӧ�����ӷ���ʽ��
��5���õ���ʽ��ʾԪ�آ�����γɻ�����Ĺ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��黯�����У���ѧ��������ȫ��ͬ���ǣ�(����)
A. HCl ��NaOHB. Na2O ��Na2O2
C. CO2�� CaOD. CaCl2�� Na2S
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з����б�ʾ��������չ������ǣ� ��
A.K��L��M��N
B.s��p��d��f
C.px��py��pz
D.������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У���Ϊͬλ�ص��� �� ��
A. ���⡢������ B. ���������� C. ���ס����� D. ���ᡢ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ���NaClO3��ȡClO2���壬����ClO2�Ƶ�NaClO2 �� ʵ��װ����ͼ��ʾ���ش��������⣺ 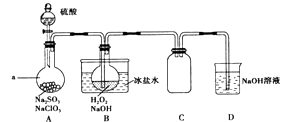
��1������a������Ϊ��װ��C�������� ��
��2����ʵ�����ʹNaClO3��������Ŀ���� ��
��3��ΪʹClO2�����ܱ����ȡ�������գ�����ʱӦע�� ��
��4��NaOH����ClO2β�����������ʵ���֮��Ϊ1��1�����������ӣ�һ��ΪClO2�� �� ����һ��Ϊ ��
��5��B�з�Ӧ�����ӷ���ʽΪ ��
��6��֤��NaClO2���������Եķ����ǣ���B����Һ���ȳ�ȥH2O2 �� ����������ţ���ͬ���ữ���ټ������飮 ��ϡHNO3��ϡH2SO4��K2SO3��Һ ��BaCl2��Һ ��FeCl2��Һ ��KSCN��Һ
��7��Ԥ��NaClO3ת��ΪNaClO2��ת����Ϊ80%����Ҫ�Ƶ�28.9g NaClO23H2O�����������144.5����������g NaClO3�����������106.5����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com