
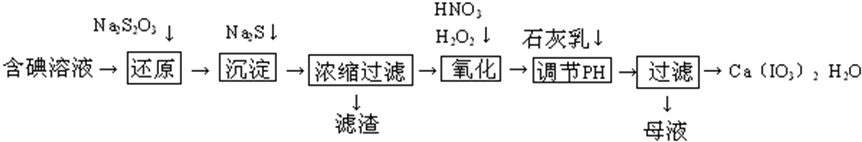
分析 I2和CuSO4溶液中加入硫代硫酸钠还原生成Na2S4O6,同时有CuI生成,再加入硫化钠产生硫化亚铜沉淀,过滤后在滤液中加入双氧水和硝酸将碘离子氧化成碘酸根,再加石灰乳,过滤得Ca(IO3)2,滤液可以循环利用,
(1)在反应2Na2S2O3+I2=Na2S4O6+2NaI中,碘的化合价降低,所以NaI是还原产物,根据化合价的变化可以计算出转移电子数目;
(2)结合所给溶解度,利用沉淀转化原理书写;硝酸具有强氧化性,Cu2S中两种元素化合价都变,可将其作一整体,然后运用守恒的思想配平;
(3)依据双氧水具有氧化性,且其还原产物为绿色无污染回答;
(4)依据所给信息“Ca(IO3)2微溶于水,可溶于硝酸”回答即可;
(5)电解时,阴极上氢离子放电,阳极上碘离子放电;依据方程式计算碘酸钙的质量.
解答 解:I2和CuSO4溶液中加入硫代硫酸钠还原生成Na2S4O6,同时有CuI生成,再加入硫化钠产生硫化亚铜沉淀,过滤后在滤液中加入双氧水和硝酸将碘离子氧化成碘酸根,再加石灰乳,过滤得Ca(IO3)2,滤液可以循环利用,
(1)反在反应2Na2S2O3+I2=Na2S4O6+2NaI中,碘的化合价降低,所以NaI是还原产物,每生成1mol的NaI,转移的电子数目约为6.02×1023,
故答案为:6.02×1023;
(2)由于Ksp(CuI)=1.1×10-12,Ksp(Cu2S)=2.5×10-48,硫化亚铜比CuI更难溶,故加入足量的Na2S除去CuI的方程式为:2CuI+Na2S=Cu2S+2NaI,在Cu2S中:Cu和S元素化合价均升高,而HNO3中N+5→+2化合价降低3,根据化合价的升降守恒得:Cu2S+12H ++10NO3- $\frac{\underline{\;\;△\;\;}}{\;}$2Cu2++SO42-+10NO2↑+6H2O,
故答案为:2CuI+Na2S=Cu2S+2NaI; Cu2S+12H ++10NO3- $\frac{\underline{\;\;△\;\;}}{\;}$2Cu2++SO42-+10NO2↑+6H2O;
(3)浓硝酸的还原产物会对大气造成污染,双氧水也具有氧化性,且还原产物为水,无污染,
故答案为:可以减少生成污染空气的氮的氧化物;
(4)Ca(IO3)2微溶于水,可溶于硝酸,即在酸性溶液中,Ca(IO3)2部分溶解;在碱性溶液中,可能会混有少量微溶的Ca(OH)2 造成产品不纯,
故答案为:在酸性溶液中,Ca(IO3)2部分溶解在硝酸;在碱性溶液中,可能会混有少量微溶的Ca(OH)2 造成产品不纯;
(5)电解时,阴极上氢离子放电生成氢气,阳极上碘离子放电生成KIO3,电极反应为:I--6e-+3H2O=IO3-+6H+,每1kgKI理论上可生产纯度为88.8%Ca(IO3)2的质量设为x,可以依据元素守恒计算,
2KI~Ca(IO3)2
332 390
1kg x×88.8%
x=1.32kg,
故答案为:3H2O+I--6e-=IO3-+6H+; 1.32.
点评 本题主要以无机物的制备流程为载体,考查的是氧化还原反应方程式书写以及配平、电解原理的应用等,综合性较强,有一定难度.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三上学期月考一化学试卷(解析版) 题型:选择题
下列有关物质的性质或应用的说法正确的是
A.晶体硅具有半导体性质,可用于生成光导纤维
B.用Na2O2漂白过的织物、麦秆日久又渐渐变成黄色
C.K2FeO4具有强氧化性,可用于自来水的杀菌消毒、
D.浓硫酸具有较强酸性,常用作淀粉水解的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体[A12(SO4)3•18H2O].
利用废铝箔(主要成分为Al、少量的Fe、Si等)既可制取有机合成催化剂AlBr3又可制取净水剂硫酸铝晶体[A12(SO4)3•18H2O].查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
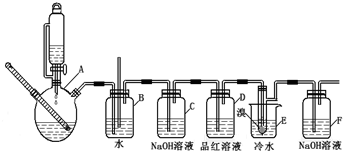
 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如图:按下列合成步骤回答问题:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如图:按下列合成步骤回答问题:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶[来 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com